
 ; CO2分子中C原子与O原子之间形成2对共用电子对,其电子式为
; CO2分子中C原子与O原子之间形成2对共用电子对,其电子式为 ,
, ;
; ;
; ,Na、Cl结合形成的化合物为NaCl,由钠离子与氯离子过程,其电子式为
,Na、Cl结合形成的化合物为NaCl,由钠离子与氯离子过程,其电子式为 ,故答案为:
,故答案为: ;
; ;
;

科目:高中化学 来源: 题型:
| A、0.15mol?L-1 |
| B、0.2mol?L-1 |
| C、0.3mol?L-1 |
| D、0.4mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
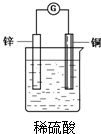 把一块锌片和一块铜片平行地插入盛有稀硫酸溶液的烧杯中,观察到的现象是
把一块锌片和一块铜片平行地插入盛有稀硫酸溶液的烧杯中,观察到的现象是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| n[(CN)2]/mol | 0.1 | 0.2 | 0.3 |
| c(SCN-)/mol?L-1 | 2 | a | 0 |
| c(Br-)/mol?L-1 | 1 | 1 | 1 |
| c(I-)/mol?L-1 | 1 | 0 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 常温下,A是黄绿色气体,B、C、D都是含A元素的化合物,转化关系如图所示.
常温下,A是黄绿色气体,B、C、D都是含A元素的化合物,转化关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com