
| A. | 亚油酸是一种植物油,常温下呈液态 | |
| B. | 1mol亚油酸可以与3molH2反应 | |
| C. | 亚油酸能使溴的四氯化碳溶液褪色 | |
| D. | 亚油酸可与NaOH溶液发生皂化反应 |
科目:高中化学 来源: 题型:选择题
| A. | 工业上海水提镁涉及的一系列反应都是氧化还原反应 | |
| B. | 汽车尾气污染物中含有的氮氧化物,是汽油或柴油不完全燃烧造成的 | |
| C. | 江河入海口形成的三角洲与胶体聚沉有关 | |
| D. | 用于光缆通信的光导纤维和制作航天服的聚酯纤维都是新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2NH3+H2SO4(浓)═(NH4)2SO4 | |
| B. | C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2SO2↑+2H2O | |
| C. | Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O | |
| D. | 2FeO+4H2SO4(浓)═Fe2(SO4)3+SO2↑+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Penguinone分子 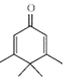 所有碳原子不可能都在同一个平面上 所有碳原子不可能都在同一个平面上 | |
| B. | 1mol  分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为5 mol、3 mol、1 mol 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为5 mol、3 mol、1 mol | |
| C. | 醋酸和软脂酸互为同系物,C5H12和C9H20也一定互为同系物 | |
| D. | 石油的裂化、裂解属于化学变化,煤的气化、液化则属于物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子间作用力 | B. | 氢键 | C. | 非极性共价键 | D. | 极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯乙烷与水互不相溶 | |
| B. | 氯乙烷中含有两种官能团 | |
| C. | 氯乙烷在一定条件下能发生消去反应 | |
| D. | 氯乙烷的结构只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅晶体是一种重要的半导体材料,在常温下,单质硅易与氧气反应,所以自然界中不存在游离态的硅.石墨烯作为目前发现的最薄、强度最大、导电导热性能最强的一种新型纳米材料,最有潜力的应用是成为硅的替代品用来生产未来的超级计算机 | |
| B. | 电解水制氢比光催化还原水制氢更节能环保、更经济 | |
| C. | 为迎接G20峰会,全温州市努力植树造林,节能减排防治PM2.5,PM2.5是指大气中直径小于或等于2.5纳米的可吸入颗粒物 | |
| D. | 某些铝硅酸盐形成的分子筛中有许多笼状空穴和通道,常用于分离、提纯气体或液体混合物,还可作干燥剂、离子交换剂、催化剂及催化剂载体等 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
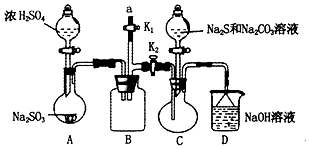 硫代硫酸钠(Na2S2O3)是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性条件下易分解,在空气中易被氧化.某化学兴趣小组通过如图装置(省略夹持装置)制备Na2S2O3.
硫代硫酸钠(Na2S2O3)是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性条件下易分解,在空气中易被氧化.某化学兴趣小组通过如图装置(省略夹持装置)制备Na2S2O3.| 实验序号 | 溶液pH | 亚硫酸钠与水的质量比 | 反应温度 | 硫粉质量 | 亚硫酸钠转化率 |
| 1 | 10 | 1.5:1 | 100℃ | 18 | 80.7% |
| 2 | 10 | 1.1:1 | 100℃ | 18 | 94.6% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使pH试纸变深蓝色的溶液:Na+、AlO2-、S2-、CO32- | |
| B. | Na2S溶液中:K+、Na+、NO3-、Ag+ | |
| C. | 含有大量Al3+的水溶液中:Na+、NH4+、HCO3-、Br- | |
| D. | 水电离产生的H+浓度为1×10-12mol•L-1的溶液:NH4+、Na+、Cl-、CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com