
���� ��1������ϡ����������ų���˵��ԭ��Һ����CO32-��
��2����1���м���һ����Ba��OH��2��Һ��������ɫ�������ó���ΪFe��OH��3�����������ܽ⣬˵���������ӣ�
��3����ɫ��������������ϡ�������ȫ���ܽ⣬˵�������в��������ᱵ��
��4������ȡ�������������������ˮ�������ȫ���ܽ⣬�õ�������Һ��
��� �⣨1������ϡ����������ų���˵��ԭ��Һ����CO32-��
��2����1���м���һ����Ba��OH��2��Һ��������ɫ�������ó���ΪFe��OH��3�����������ܽ⣬˵���������ӣ�
��3����ɫ��������������ϡ�������ȫ���ܽ⣬˵�������в��������ᱵ��
��4������ȡ�������������������ˮ�������ȫ���ܽ⣬�õ�������Һ��
��ˣ�һ�������е�������SO42-��CO32-���϶����е�������Fe3+��Al3+��Cl-����ʵ��û���漰��K+������ȷ���Ƿ��е�������K+����ͨ����ɫ��Ӧ���м���
�ʴ�Ϊ��SO42-��CO32-��Fe3+��Al3+��Cl-��K+����ɫ��Ӧ��
���� ���⿼�鳣�����ӵļ��飬��Ŀ�Ѷ��еȣ�����ע��ͨ����Ӧ��ʵ�������жϣ��������ʵĵ������ʣ���Ϊ�ƶϵ�ͻ�ƿڣ�


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���ڶ�����̼
���ڶ�����̼ �����Ȼ�þ���γɹ��̣�
�����Ȼ�þ���γɹ��̣� ���ܴ�������γɹ��̣�
���ܴ�������γɹ��̣� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ѡ�� | ��Ⱦ�� | ������ʩ | ������� |
| A | ���Եķ�ˮ | ��CO2�к� | ��ѧ�� |
| B | Cu2+���ؽ������� | �������γ��� | ��ѧ�� |
| C | �������л���ķ�ˮ | ͨ�������л | ������ |
| D | ���� | ����ʯ���к� | ��ѧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
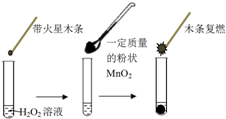 �о������Ի�ѧ��Ӧ����Ҫ���壮Ϊ̽��������˫��ˮ�ֽ�Ĵ�Ч����ij�о�С����������ʵ�飺
�о������Ի�ѧ��Ӧ����Ҫ���壮Ϊ̽��������˫��ˮ�ֽ�Ĵ�Ч����ij�о�С����������ʵ�飺| MnO2������/g | 0.1 | 0.2 | 0.4 |
| 40sĩO2���/mL | 49 | 61 | 86 |
| �Թ� | �� | �� | �� |
| �μ��Լ� | 5��0.1mol•L-1FeCl3 | 5��0.1mol•L-1 CuCl2 | 5��0.3mol•L-1 NaCl |
| ����������� | �Ͽ����ϸС���� | ��������ϸС���� | �����ݲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� �� | Fe��OH��2 | Cu��OH��2 | Fe��OH��3 |
| �ܶȻ�/25�� | 8.0��10-16 | 2.2��10-20 | 4.0��10-38 |
| ��ȫ����ʱ��pH��Χ | ��9.6 | ��6.4 | 3��4 |
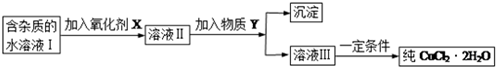
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com