
| A. | 热稳定性:碘化氢>溴化氢>氯化氢 | B. | 氧化性:K+<Na+ | ||
| C. | 最高正化合价:氯>硫>磷 | D. | 原子半径:钠>硫>氯 |
分析 A.非金属越强,气态氢化物越稳定;
B.金属性越强,其对应阳离子的氧化性越弱;
C.Cl、S、P的最高化合价等于其最外层电子数;
D.同一周期,自左到右,原子半径逐渐减小.
解答 解:A.因为非金属性Cl>Br>I,所以热稳定性HCl>HBr>HI,故A错误;
B.因此金属性>Na,金属性越强,其对应阳离子的氧化性越弱,所以氧化性K+<Na+,故B正确;
C.P、S、Cl的最外层电子数分别是5、6、7,最高化合价分别为+5、+6、+7,故C正确;
D.同一周期,自左到右,原子半径逐渐减小,原子半径:钠>硫>氯,故D正确;
故选A.
点评 本题考查元素周期表和元素周期律,为高频考点,把握同周期和同主族元素的性质变化规律、金属性与非金属性强弱的比较方法是解答本题的关键,题目难度不大.


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 所有卤代烃都是难溶于水、密度比水小的液体 | |
| B. | 所有卤代烃在常温下都是液体,且都是非电解质 | |
| C. | 所有卤代烃都含有卤原子 | |
| D. | 所有卤代烃都是通过取代反应制得的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

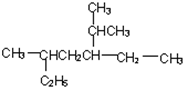 2,5-二甲基-3-乙基-庚烷
2,5-二甲基-3-乙基-庚烷 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应中的能量变化都表现为热量的变化 | |
| B. | 应用盖斯定律,可计算某些难以直接测量的反应焓变 | |
| C. | 反应物的总能量低于生成物的总能量时,发生吸热反应 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用SO2漂白纸浆和草帽辫 | |
| B. | SO2具有强还原性,浓硫酸具有强氧化性,故浓硫酸不能用于干燥SO2气体 | |
| C. | 将浓硫酸滴到蔗糖表面,固体变黑膨胀,说明浓硫酸有脱水性和强氧化性 | |
| D. | Na2SO3与H2O2的反应为氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③>①>②>④ | B. | ④>③>①>② | C. | ③>①=④>② | D. | ①=③=④>② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
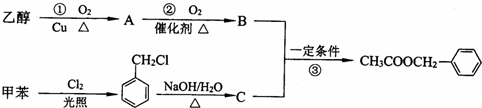
 .
.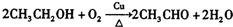 ..
.. 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 组成上相差一个或若干个CH2 原子团,且符合同一通式的有机物之间互称为同系物 | |
| B. | 苯分子结构中不存在碳碳双键,因此苯不能发生加成反应 | |
| C. | 相同条件下,正丁烷、正戊烷、正己烷的沸点依次减小 | |
| D. | 皮肤上不小心沾上苯酚的浓溶液可用酒精清洗 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com