
| A���ܱ������У�9.6g�����11.2g���ۻ�ϼ�������������17.6gʱ���ų�19.12kJ��������Fe��s��+S��s���TFeS��s����H=-95.6kJ��mol-1 |
| B��ϡ������0.1mol?L-1NaOH��Һ��Ӧ��H+��aq��+OH-��aq���TH2O��l����H=57.3kJ?mol-1 |
| C����֪1mol������ȫȼ������Һ̬ˮ���ų�������Ϊ285.5kJ����ˮ�ֽ���Ȼ�ѧ����ʽ��2H2O��l���T2H2��g��+O2��g����H=+285.5kJ��mol-1 |
| D����֪2C��s��+O2��g���T2CO��g����H=-22.1kJ��mol-1���֪C��ȼ���ȡ�H=-110.5kJ��mol-1 |
| 1 |
| 0.2 |


 �����ߴ���ϵ�д�
�����ߴ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��H2��F2��Ӧ���Ȼ�ѧ����ʽΪ��H2��g��+F2��g��=2HF��g����H=-541kJ |
| B��44.8LHF����ֽ��22.4LH2��22.4LF2����541kJ������ |
| C��1molH2��1molF2��Ӧ����2molҺ̬HF�ų�������С��541kJ |
| D������ͬ�����£�1molH2��1molF2�������ܺʹ���2molHF��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ȷ�Ӧ����Ҫ���ȾͿ��Է��� |
| B����ѧ��Ӧ���������������⣬�������������ı仯 |
| C����Ӧ����Ϊ���ȵķ�Ӧ�������ȷ�Ӧ |
| D����ѧ��Ӧ���Ȼ������ȣ�ȡ���ڷ�Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
| 1 |
| 2 |
| 2 |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��CH3OH��l��+
| ||
| B��2CH3OH��l��+3O2��g���T2CO2��g��+4H2O��l����H=-1452kJ?mol-1 | ||
C��CH3OH��l��+
| ||
D��CH3OH��l��+
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
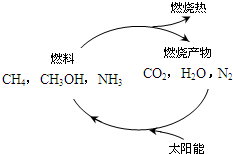
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
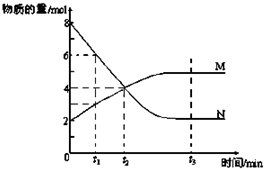
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��һ���¶��£���ӦMgCl2(l)=Mg(l)��Cl2(g)�Ħ�H>0 ��S>0 |
| B�����Ƿ��ȷ�Ӧ�����Է��ģ��������ȷ�Ӧ���Ƿ��Է��� |
C�������£�2H2O 2H2����O2������������ˮ�ķֽⷴӦ���Է���Ӧ 2H2����O2������������ˮ�ķֽⷴӦ���Է���Ӧ |
| D�����ڷ�ӦH2O2=2H2O��O2��������MnO2�������¶ȶ��ܼӿ�O2���������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com