
| A. | 16g氧气中所含的氧原子数为NA | |
| B. | 1molCl2与足量H2O反应,转移的电子数为2NA | |
| C. | 标准状况下,22.4L二氧化硅所含有的原子数目为3NA | |
| D. | 钠在氧气中燃烧,1 mol O2作氧化剂时得到的电子数为4NA |
分析 A、氧气分子由氧原子构成;
B、氯气和水的反应为可逆反应;
C、标况下二氧化硅为固体;
D、氧气和钠反应后变为-1价.
解答 解:A、氧气分子由氧原子构成,故16g氧气中含有的氧原子的物质的量为n=$\frac{16g}{16g/mol}$=1mol,个数为NA个,故A正确;
B、氯气和水的反应为可逆反应,不能进行彻底,且反应为歧化反应,故转移的电子数小于NA个,故B错误;
C、标况下二氧化硅为固体,故不能根据气体摩尔体积来计算其物质的量和原子个数,故C错误;
D、氧气和钠反应后变为-1价,故1mol氧气得到2mol电子即2NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 尿素CO(NH2)2 | B. | NH4NO3 | C. | NH4HCO3 | D. | (NH4)2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
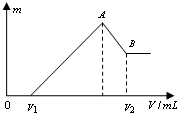 将0.1mol的镁、铝混合物溶于100mL 2mol/LH2SO4溶液中,然后再滴加1mol/L NaOH溶液.请回答:
将0.1mol的镁、铝混合物溶于100mL 2mol/LH2SO4溶液中,然后再滴加1mol/L NaOH溶液.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯离子的结构示意图: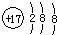 | |
| B. | 作为相对原子质量测定标准的碳核素:${\;}_6^{14}$C | |
| C. | 氯化镁的电子式: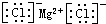 | |
| D. | 乙烯结构简式CH2=CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸式滴定管未用待测盐酸润洗 | |
| B. | 碱式滴定管未用标准碱液润洗 | |
| C. | 锥形瓶用蒸馏水洗净后未用待测液润洗 | |
| D. | 滴定前仰视读数,滴定后平视读数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ•mol-1 | |
| B. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ•mol-1 | |
| C. | CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-725.8kJ•mol-1 | |
| D. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=+1452kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 配料 | 食盐、碘酸钾、抗结剂 |
| 碘含量 | 35±15mg/kg |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入碘盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com