
常温下,下列溶液中微粒的物质的量浓度关系一定正确的是
A.NaHCO3溶液中:c(H+) +c(H2CO3)=2c(CO32-) +c(OH-)
B.向0.1mol·L-1的NH4Cl溶液中通入一定量的NH3后:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.向CH3COOH溶液中滴加NaOH使pH>7溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.0.3mol·L-1的HY溶液与0.3mol·L-1的NaOH溶液等体积混合后所得pH=9的溶液中:c(OH-)-c(HY)=c(H+)=1×10-9mol·L-1
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016届四川省宜宾县高三第一次适应性测试理综化学试卷(解析版) 题型:实验题
亚氯酸钠(NaClO2)是重要漂白剂,探究小组开展如下实验,请回答:
[实验Ⅰ]NaClO2晶体按如下图装置进行制取。
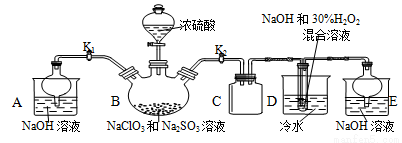
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2,
高于60℃时NaClO2分解成NaClO3和NaCl。
(1)装置C起的是 的作用。
(2)已知装置B中的产物有ClO2气体,装置D中生成NaClO2和一种助燃气体,其反应的化学方程式为 。
(3)从装置D反应后的溶液中获得NaClO2晶体的操作步骤为:①减压在55℃蒸发结晶;
② ;③用38℃~60℃热水洗涤;④低于 ℃干燥;得到成品。.
(4)反应结束后,打开K1,装置A起的作用是 ;如果撤去D中的冷水浴,可能导致
产品中混有的杂质是 。
[实验Ⅱ]样品杂质分析与纯度测定
(5)测定样品中NaClO2的纯度:准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2﹣+4I﹣+4H+=2H2O+2I2+Cl﹣,将所得混合液稀释成100mL待测溶液。取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol•L﹣1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2+2S2O32﹣=2I﹣+S4O62﹣),则所称取的样品中NaClO2的物质的量为 。
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三5月模拟一理综化学试卷(解析版) 题型:选择题
下列根据实验操作和现象所得出的结论不正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向某溶液中加入盐酸酸化的BaCl2溶液 | 有白色沉淀生成 | 溶液中不一定含有SO42- |
B | 向Fe(NO3)2溶液中滴入H2SO4酸化的H2O2溶液 | 溶液变为黄色 | 氧化性:H2O2﹥Fe3+ |
C | 将新制氯水和NaBr溶液在试管中混合后,加入CCl4,振荡静置 | 下层呈红棕色 | 氧化性:Cl2﹥Br2 |
D | 向0.1mol·L-1 AgNO3溶液中滴入稀盐酸至不再有沉淀产生,再滴加0.1mol·L-1 NaI溶液 | 先有白色沉淀后变为黄色沉淀 | Ksp:AgI<AgCl |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南嘉积中学高二下期中理科化学试卷(解析版) 题型:选择题
下列变化中,由加成反应引起的是
A.乙烯通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色
B.苯在一定温度、压强和催化剂的作用下和氢气反应,生成环己烷
C.一定条件下,苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成
D.由电石制乙炔
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三下学期考前练习化学试卷(解析版) 题型:实验题
ClO2气体是一种高效、广谱、安全的杀菌消毒剂,可用NaClO3和草酸(H2C2O4)反应制得,无水草酸100℃可以升华,某学习小组用下图装置模拟工业制取收集ClO2。

(1)实验时装置A需在60℃~100℃进行的原因是______________,控制所需温度的方法是__________;
(2)电动搅拌棒的作用是______________,装置A中反应产物有Na2CO3、ClO2和CO2等,该反应的化学方程式为_________________;
(3)在装置C中ClO2和NaOH反应生成等物质的量的两种盐,其中一种盐为NaClO2,写出反应的离子方程式_________________;
(4)用ClO2处理过的饮用水(pH为5.5~6.5)往往残留少量ClO2和一定量对人体不利的亚氯酸根离子(ClO2-).
①ClO2被I-还原为ClO2-、Cl-的转化率与溶液pH的关系如图2所示
②当pH≤2.0时,ClO2-也能被I-还原成Cl-
③2Na2S2O3+I2=Na2S4O6+2NaI
根据上述信息,请补充完整测定饮用水中ClO2-含量的实验方案:
取一定体积的饮用水,加入NaOH溶液调节pH为7.0~8.0;______________________________________
_________________________________________________________________________________;再重复上述操作1~2次,计算得出结果。
(实验中需使用的试剂:淀粉溶液、标准Na2S2O3溶液、KI溶液、稀硫酸)
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三下学期考前练习化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.氨水溶解氯化银沉淀:AgCl+2NH3•H2O=[Ag(NH3)2]++Cl-+2H2O
B.CH3COOH溶液除去水垢中的CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
C.酸性K2Cr2O7溶液氧化双氧水:Cr2O72-+8H++5H2O2=2 Cr3++4O2↑+9H2O
D.将NaHSO4与Ba(OH)2溶液混合至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三下学期考前练习化学试卷(解析版) 题型:选择题
下列有关化学用语正确的是
A.中子数为18的硫原子:3416S
B.氨分子的电子式: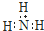
C.苯乙酸钠的结构简式: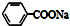
D.H2SO3的电离方程式:H2SO3?2H++SO32
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都石室中学高二4月月考化学试卷(解析版) 题型:填空题
火力发电厂释放出大量氮氧化合物(NOx)、SO2和 CO2等气体会造成环境问题对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
CH4(g)+ 4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160kJ/mol
甲烷直接将NO2还原为N2的热化学方程式为____________________。
(2)脱碳。将 CO2转化为甲醇:CO2 (g)+3H2 (g)  CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
①如图 1,25℃时以甲醇燃料电池(电解质溶液为 KOH)为电源来电解乙(100mL2mol/LAgNO3溶液)和丙(100mLCuSO4)溶液,燃料电池负极的电极反应为_______________。电解结束后,向丙中加入 0.1mol Cu(OH)2,恰好恢复到反应前的浓度,将乙中溶液加水稀释至200mL,溶液的 pH ______________;

②取五份等体积的 CO2和H2的混合气体(物质的量之比均为 1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数 φ (CH3OH)与反应温度 T 的关系曲线如图 2 所示,则上述 CO2转化为甲醇的反应的△H________3.0 (填“>”、“<”或“=”)。
(3)脱硫。燃煤废气经脱硝、脱碳后,与一定量氨气、空气反应生成硫酸铵。室温时,向(NH4)2SO4,溶液中滴人 NaOH 溶液至溶液呈中性,则所得溶液中微粒浓度大小关系c(Na+)________ c(NH3 •H2O)。(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三下最后一次模拟理综化学试卷(解析版) 题型:填空题
铁及其化合物在工农业生产、环境保护等领域中有着重要的作用。
(1)硫酸铁铵[NH4Fe(SO4)2·12H2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。写出硫酸铁铵溶液中离子浓度的大小顺序 。
(2)FeSO4/KMnO4工艺与单纯混凝剂[FeCl3、Fe2(SO4)3]相比,大大降低了污水处理后水的浑浊度,显著提高了对污水中有机物的去除率。二者的引入并未增加沉降后水中总铁和总锰浓度,反而使二者的浓度降低,原因是在此条件下(pH约为7)KMnO4可将水中Fe2+、Mn2+氧化为固相的+3价铁和+4价锰的化合物,进而通过沉淀、过滤等工艺将铁、锰除去。已知:Ksp(Fe(OH)3=4.0×10-38,则沉淀过滤后溶液中c(Fe3+)约为 mol·L-1。写出生成+4价固体锰化合物的反应的离子方程式 。
(3)新型纳米材料ZnFe2Ox,可用于除去工业废气中的某些氧化物。制取新材料和除去废气的转化关系如图:
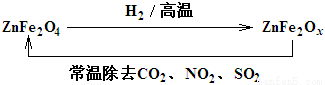
用ZnFe2Ox除去SO2的过程中,氧化剂是 。(填化学式)
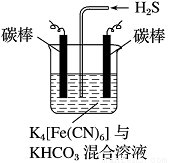
(4)工业上常采用如图所示电解装置,利用铁的化合物将气态废弃物中的硫化氢转化为可利用的硫。先通电电解,然后通入H2S时发生反应的离子方程式为:2[Fe(CN)6]3-+2CO+H2S=2[Fe(CN)6]4-+2HCO+S↓。电解时,阳极的电极反应式为 ;电解过程中阴极区溶液的pH (填“变大”、“变小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com