
【题目】硫代硫酸钠(Na2S2O3)是常用的还原剂。在一定体积的某维生素C(化学式C6H8O6)溶液中加入a mol·L-1I2溶液V1 mL,使维生素C完全氧化,充分反应后,用Na2S2O3溶液滴定剩余的I2,消耗b mol·L-1 Na2S2O3溶液V2 mL。
已知发生的反应为:C6H8O6+I2=C6H6O6+2H++2I- , 2S2O32-+I2=S4O62-+2I-
该溶液中维生素C的物质的量是多少mol?(写出简要的计算过程)。
科目:高中化学 来源: 题型:
【题目】下列有关实验操作或实验原理叙述正确的是

A.可以用pH试纸测定饱和氯水的pH
B.用10mL量筒量取8.5 mL 0.1 mol·L-1 盐酸
C.用图1所示操作检查装置的气密性
D.实验室用图2所示装置制取纯净的NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语对事实的表述不正确的是
A. 硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH![]() C17H35COOC2H5+H218O
C17H35COOC2H5+H218O
B. 常温时,0.1 mol·L-1氨水的pH=11.1:NH3·H2O![]()
![]() +OH
+OH
C. 由Na和C1形成离子键的过程:![]()
D. 电解精炼铜的阴极反应:Cu2+ +2e![]() Cu
Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、R是五种短周期元素,原子序数依次增大,X原子是所有原子中半径最小的,Y元素最高正价与最低负价之和为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素,请回答:
(1)R离子电子排布式为:_____________________。
(2)X与Q形成的化合物属于__________化合物(填“离子”或“共价”)
(3)由以上两种元素组成的化合物中,常温下呈液态的化合物A,原子比例为2:1,其结构式为__________,其熔点,沸点较高时因为分子间存在__________;呈淡黄色固体的化合物B,其电子式:__________。
(4)如果由三种元素组成化合物中,C为两性不溶物,D为强碱,则C与D反应的化学方程式为_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备三氯乙醛(CCl3CHO)的反应原理为C2H5OH+4Cl2![]() CCl3CHO+5HCl,可能发生的副反应是C2H5OH+HCl
CCl3CHO+5HCl,可能发生的副反应是C2H5OH+HCl![]() C2H5Cl+H2O。某探究小组模拟制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。
C2H5Cl+H2O。某探究小组模拟制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。
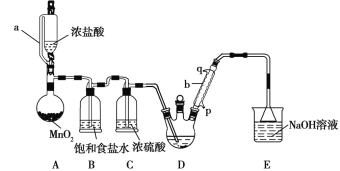
回答下列问题:
(1)用仪器a代替普通分液漏斗的目的是_______________。
(2)装置A中MnO2可以用KMnO4代替,反应可以在常温下进行,试写出反应的离子方程式__。
(3)仪器b中冷凝水从___(填“p”或“q”,下同)口进,___口出。
(4)若撤去装置B,对实验的影响是______________。
(5)实验时发现D中导管口处气泡速率过快,合理的解决方法是___________。
(6)已知:CCl3CHO+OH-![]() CHCl3+HCOO-;HCOO-+I2
CHCl3+HCOO-;HCOO-+I2![]() H++2I-+CO2↑;I2+2S2O32-
H++2I-+CO2↑;I2+2S2O32-![]() 2I-+S4O62-。称取0.40 g产品,配成待测溶液,加入20.00 mL 0.100 mol·L-1碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020 mol·L-1的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00 mL。滴定时所用指示剂是___________,达到滴定终点时的现象是_________________,测得该产品的纯度为_____(保留一位小数)。
2I-+S4O62-。称取0.40 g产品,配成待测溶液,加入20.00 mL 0.100 mol·L-1碘标准溶液,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,并立即用0.020 mol·L-1的Na2S2O3溶液滴定至终点。重复上述操作3次,平均消耗Na2S2O3溶液20.00 mL。滴定时所用指示剂是___________,达到滴定终点时的现象是_________________,测得该产品的纯度为_____(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中实线是元素周期表的部分边界,其中上边界并未用实线标出。
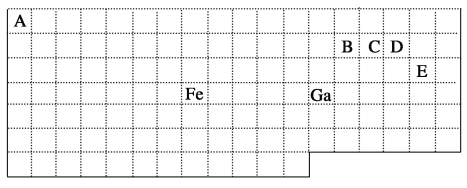
根据信息回答下列问题:
(1)周期表中基态Ga原子的最外层电子排布式为___________。
(2)Fe元素位于周期表的________分区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为_______。
(3)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有________。
(4)根据VSEPR理论预测ED4-的空间构型为________。B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子的分子式为_________(写2种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别取浓度不同、体积均为20.00mL的3种HCl溶液,分别滴入浓度为1.000mol·L-1,0.1000mol·L-1和0.01000mol·L-1的NaOH溶液,测得3个反应体系的pH随V(NaOH)的变化的曲线如图,在V(NaOH)=20.00mL前后出现突跃。下列说法不正确的是

A. 3种HCl溶液的c(HCl):最大的是最小的100倍
B. 曲线a、b、c对应的c(NaOH):a>b>c
C. 当V(NaOH)=20.00mL时,3个体系中均满足:c(Na+)=c(Cl-)
D. 当V(NaOH)相同时,pH突跃最大的体系中的c(H+)最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )

A. KO2中只存在离子键
B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2-
C. 晶体中与每个K+距离最近的O2-有6个
D. 晶体中,所有原子之间都以离子键相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】混合动力汽车(HEV)中使用了镍氢电池,其工作原理如图所示其中M为储氢合金,MH为吸附了氢原子的储氢合金,KOH溶液作电解液。关于镍氢电池,下列说法不正确的是

A. 充电时,阴极附近pH降低
B. 电动机工作时溶液中OH-向甲移动
C. 放电时正极反应式为: NiOOH+H2O+e- = Ni(OH)2+OH-
D. 电极总反应式为:M+Ni(OH)2 = MH+NiOOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com