

分析 (1)图中甲池能自发进行氧化还原反应,属于原电池,通燃料的电极是负极,通氧气的电极是正极;
(2)通入甲醇的电极为负极、通入氧气的电极为正极,电解池中连接原电池负极的电极为阴极、连接原电池正极的电极为阳极;
(3)甲醇失电子和氢氧根离子反应生成碳酸根离子和水;
(4)乙池中A电极上氢氧根离子放电、阴极上银离子放电,据此书写乙池中反应的化学方程式;
(5)根据转移电子相等结合电极反应式进行计算.
解答 解:(1)图中甲池能自发进行氧化还原反应,将化学能转化为电能,属于原电池,故答案为:原电池;
(2)通入甲醇的电极为负极、通入氧气的电极为正极,A连接原电池正极,为电解池阳极,故答案为:阳极;
(3)甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH3OH-6e-+8OH-═6H2O+CO32-,故答案为:CH3OH-6e-+8OH-═6H2O+CO32-;
(4)乙池中A电极上氢氧根离子放电、阴极上银离子放电,所以乙池电池反应式为4AgNO3+2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4HNO3,
故答案为:4AgNO3+2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4HNO3;
(5)B(Ag)极的质量增加5.4g时,n(Ag)=$\frac{5.4g}{108g/mol}$=0.05mol,则转移电子为0.05mol,根据转移电子相等,甲池中理论上消耗O2的体积=$\frac{0.05mool}{4}$×22.4L/mol=0.28L,此时丙池中某电极析出1.6g某金属,转移电子为0.05mol,所以金属的摩尔质量是64g/mol,所以电解质是含有铜离子的盐溶液,故选B.
故答案为:0.28;B.
点评 本题考查了原电池和电解池原理,为高频考点,涉及电极反应式的书写及物质的量的金属,会结合电解质溶液酸碱性书写电极反应式,再结合转移电子相等进行计算,题目难度不大.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 | |
| B. | “丹砂(HgS)烧之成水银,积变又还成了丹砂”,该过程发生了分解、化合、氧化还原反应 | |
| C. | 干燥剂硅胶和硅橡胶的主要化学成分都是二氧化硅 | |
| D. | 铜制品在潮湿的空气中生锈,其主要原因是发生了析氢腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
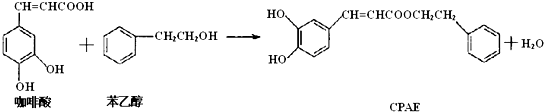
| A. | 咖啡酸分子中所有原子不可能处在同一个平面上 | |
| B. | 可用金属Na检测上述反应是否残留苯乙醇 | |
| C. | 1mol 苯乙醇在O2中完全燃烧,需消耗10molO2 | |
| D. | 1mol CPAE与足量的NaOH溶液反应,最多消耗3molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b>c>d | B. | a>c>d>b | C. | c>a>b>d | D. | b>d>c>a |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 已知条件 | 热化学方程式 | |
| A | CH4的燃烧热(△H)为-890kJ• mol-1 | CH4(g)+2O2(g)═CO2(g)+2H2O(g) △H=-890kJ• mol-1 |
| B | 中和热△H=-57.3kJ•mol-1 | CH3COOH(aq)+NaOH(aq)═H2O+CH3COONa (aq)△H=-57.3kJ•mol-1 |
| C | 一定条件下,0.5mol N2与1.5mol H2充分反应后放出30.5kJ的热量 | N2(g)+3H2(g)?2NH3(g)△H=-61kJ•mol-1 |
| D | 96g O2的能量比96g O3的能量低bkJ | 3O2(g)?2O3(g)△H=+bkJ• mol-1 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al--Al2O3--Al(OH)3--Na[Al(OH)4] | B. | Mg--MgCl2--Mg(OH)2--MgO | ||
| C. | S--SO3--H2SO4--MgSO4 | D. | Si--SiO2--H2SiO3--Na2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com