
 £®
£®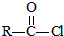
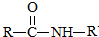 $\stackrel{NaOHČÜŅŗ}{”ś}$RCOONa+R”ä-NH2
$\stackrel{NaOHČÜŅŗ}{”ś}$RCOONa+R”ä-NH2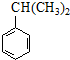 æÉ×Ŗ»ÆĪŖ1mol AŗĶ1mol B£¬ĒŅAÓėFeCl3ČÜŅŗ×÷ÓĆĻŌ×ĻÉ«£¬Š“³öAµÄĻ”ČÜŅŗÓė¹żĮæÅØäåĖ®·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½
æÉ×Ŗ»ÆĪŖ1mol AŗĶ1mol B£¬ĒŅAÓėFeCl3ČÜŅŗ×÷ÓĆĻŌ×ĻÉ«£¬Š“³öAµÄĻ”ČÜŅŗÓė¹żĮæÅØäåĖ®·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ £®
£®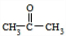 £»ĘĖČČĻ¢Ķ“µÄ½į¹¹¼ņŹ½ĪŖ
£»ĘĖČČĻ¢Ķ“µÄ½į¹¹¼ņŹ½ĪŖ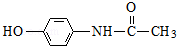 £®
£® ”ś
”ś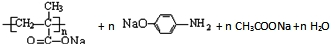 £®
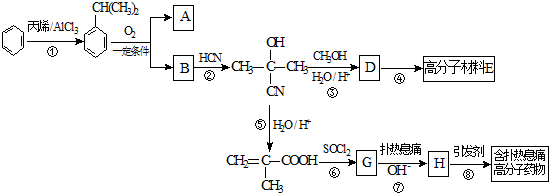
£®·ÖĪö ±½ŗĶ±ūĻ©ŌŚĀČ»ÆĀĮ“ęŌŚĢõ¼žĻĀ·¢Éś¼Ó³É·“Ӧɜ³ÉŅģ±½±ūĶ飬Ņģ±½±ūĶé±»Ńõ»ÆÉś³ÉAŗĶB£¬BŗĶĒāĒčĖį·¢Éś¼Ó³É·“Ӧɜ³É £¬ŌņBĪŖ
£¬ŌņBĪŖ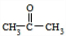 £¬1mol
£¬1mol  æÉ×Ŗ»ÆĪŖ1mol AŗĶ1mol B£¬ĒŅAÓėFeCl3ČÜŅŗ×÷ÓĆĻŌ×ĻÉ«£¬ĖµĆ÷AÖŠŗ¬ÓŠ·ÓōĒ»ł£¬øł¾ŻĢ¼Ō×ÓŹŲŗćÖŖAŹĒ
æÉ×Ŗ»ÆĪŖ1mol AŗĶ1mol B£¬ĒŅAÓėFeCl3ČÜŅŗ×÷ÓĆĻŌ×ĻÉ«£¬ĖµĆ÷AÖŠŗ¬ÓŠ·ÓōĒ»ł£¬øł¾ŻĢ¼Ō×ÓŹŲŗćÖŖAŹĒ £®
£® ·¢Éś·“Ӧɜ³ÉD£¬DÕōĘųĆܶȏĒĻąĶ¬×“Ģ¬ĻĀ¼×ĶéĆܶȵÄ6.25±¶£¬ŌņDµÄĻą¶Ō·Ö×ÓÖŹĮæŹĒ16”Į6.25=100£¬DÖŠø÷ŌŖĖŲµÄÖŹĮæ·ÖŹż·Ö±šĪŖĢ¼60%£¬Ēā8%£¬Ńõ32%£¬ŌņĢ¼”¢Ēā”¢ŃõŌ×ÓøöŹż±Č=$\frac{60%}{12}$£ŗ$\frac{8%}{1}$£ŗ$\frac{32%}{16}$=5£ŗ8£ŗ2£¬ŌņDµÄ·Ö×ÓŹ½ĪŖ£ŗC5H8O2£¬DµÄ²»±„ŗĶ¶ČĪŖ£ŗ$\frac{2”Į5+2-8}{2}$=2£¬ĖłŅŌDÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬ĒŅŗ¬ÓŠõ„»ł£¬ŌņDµÄ½į¹¹¼ņŹ½ĪŖ£ŗCH2=C£ØCH3£©COOCH3£»D·¢Éś¼Ó¾Ū·“Ӧɜ³ÉEĪŖ
·¢Éś·“Ӧɜ³ÉD£¬DÕōĘųĆܶȏĒĻąĶ¬×“Ģ¬ĻĀ¼×ĶéĆܶȵÄ6.25±¶£¬ŌņDµÄĻą¶Ō·Ö×ÓÖŹĮæŹĒ16”Į6.25=100£¬DÖŠø÷ŌŖĖŲµÄÖŹĮæ·ÖŹż·Ö±šĪŖĢ¼60%£¬Ēā8%£¬Ńõ32%£¬ŌņĢ¼”¢Ēā”¢ŃõŌ×ÓøöŹż±Č=$\frac{60%}{12}$£ŗ$\frac{8%}{1}$£ŗ$\frac{32%}{16}$=5£ŗ8£ŗ2£¬ŌņDµÄ·Ö×ÓŹ½ĪŖ£ŗC5H8O2£¬DµÄ²»±„ŗĶ¶ČĪŖ£ŗ$\frac{2”Į5+2-8}{2}$=2£¬ĖłŅŌDÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬ĒŅŗ¬ÓŠõ„»ł£¬ŌņDµÄ½į¹¹¼ņŹ½ĪŖ£ŗCH2=C£ØCH3£©COOCH3£»D·¢Éś¼Ó¾Ū·“Ӧɜ³ÉEĪŖ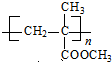 £®ÓÉ·“Ó¦ŠÅĻ¢IIæÉÖŖ
£®ÓÉ·“Ó¦ŠÅĻ¢IIæÉÖŖ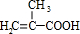 ŗĶSOCl2·¢ÉśČ”“ś·“Ӧɜ³ÉGĪŖCH2=C£ØCH3£©COCl£¬G·“Ӧɜ³ÉH£¬H·“Ӧɜ³É
ŗĶSOCl2·¢ÉśČ”“ś·“Ӧɜ³ÉGĪŖCH2=C£ØCH3£©COCl£¬G·“Ӧɜ³ÉH£¬H·“Ӧɜ³É £¬ŌņHĪŖ
£¬ŌņHĪŖ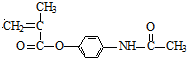 £¬¾Ż“Ė½ā“š£®
£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗ±½ŗĶ±ūĻ©ŌŚĀČ»ÆĀĮ“ęŌŚĢõ¼žĻĀ·¢Éś¼Ó³É·“Ӧɜ³ÉŅģ±½±ūĶ飬Ņģ±½±ūĶé±»Ńõ»ÆÉś³ÉAŗĶB£¬BŗĶĒāĒčĖį·¢Éś¼Ó³É·“Ӧɜ³É £¬ŌņBĪŖ
£¬ŌņBĪŖ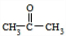 £¬1mol
£¬1mol  æÉ×Ŗ»ÆĪŖ1mol AŗĶ1mol B£¬ĒŅAÓėFeCl3ČÜŅŗ×÷ÓĆĻŌ×ĻÉ«£¬ĖµĆ÷AÖŠŗ¬ÓŠ·ÓōĒ»ł£¬øł¾ŻĢ¼Ō×ÓŹŲŗćÖŖAŹĒ
æÉ×Ŗ»ÆĪŖ1mol AŗĶ1mol B£¬ĒŅAÓėFeCl3ČÜŅŗ×÷ÓĆĻŌ×ĻÉ«£¬ĖµĆ÷AÖŠŗ¬ÓŠ·ÓōĒ»ł£¬øł¾ŻĢ¼Ō×ÓŹŲŗćÖŖAŹĒ £®
£® ·¢Éś·“Ӧɜ³ÉD£¬DÕōĘųĆܶȏĒĻąĶ¬×“Ģ¬ĻĀ¼×ĶéĆܶȵÄ6.25±¶£¬ŌņDµÄĻą¶Ō·Ö×ÓÖŹĮæŹĒ16”Į6.25=100£¬DÖŠø÷ŌŖĖŲµÄÖŹĮæ·ÖŹż·Ö±šĪŖĢ¼60%£¬Ēā8%£¬Ńõ32%£¬ŌņĢ¼”¢Ēā”¢ŃõŌ×ÓøöŹż±Č=$\frac{60%}{12}$£ŗ$\frac{8%}{1}$£ŗ$\frac{32%}{16}$=5£ŗ8£ŗ2£¬ŌņDµÄ·Ö×ÓŹ½ĪŖ£ŗC5H8O2£¬DµÄ²»±„ŗĶ¶ČĪŖ£ŗ$\frac{2”Į5+2-8}{2}$=2£¬ĖłŅŌDÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬ĒŅŗ¬ÓŠõ„»ł£¬ŌņDµÄ½į¹¹¼ņŹ½ĪŖ£ŗCH2=C£ØCH3£©COOCH3£»D·¢Éś¼Ó¾Ū·“Ӧɜ³ÉEĪŖ
·¢Éś·“Ӧɜ³ÉD£¬DÕōĘųĆܶȏĒĻąĶ¬×“Ģ¬ĻĀ¼×ĶéĆܶȵÄ6.25±¶£¬ŌņDµÄĻą¶Ō·Ö×ÓÖŹĮæŹĒ16”Į6.25=100£¬DÖŠø÷ŌŖĖŲµÄÖŹĮæ·ÖŹż·Ö±šĪŖĢ¼60%£¬Ēā8%£¬Ńõ32%£¬ŌņĢ¼”¢Ēā”¢ŃõŌ×ÓøöŹż±Č=$\frac{60%}{12}$£ŗ$\frac{8%}{1}$£ŗ$\frac{32%}{16}$=5£ŗ8£ŗ2£¬ŌņDµÄ·Ö×ÓŹ½ĪŖ£ŗC5H8O2£¬DµÄ²»±„ŗĶ¶ČĪŖ£ŗ$\frac{2”Į5+2-8}{2}$=2£¬ĖłŅŌDÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬ĒŅŗ¬ÓŠõ„»ł£¬ŌņDµÄ½į¹¹¼ņŹ½ĪŖ£ŗCH2=C£ØCH3£©COOCH3£»D·¢Éś¼Ó¾Ū·“Ӧɜ³ÉEĪŖ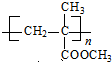 £®ÓÉ·“Ó¦ŠÅĻ¢IIæÉÖŖ
£®ÓÉ·“Ó¦ŠÅĻ¢IIæÉÖŖ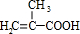 ŗĶSOCl2·¢ÉśČ”“ś·“Ӧɜ³ÉGĪŖCH2=C£ØCH3£©COCl£¬G·“Ӧɜ³ÉH£¬H·“Ӧɜ³É
ŗĶSOCl2·¢ÉśČ”“ś·“Ӧɜ³ÉGĪŖCH2=C£ØCH3£©COCl£¬G·“Ӧɜ³ÉH£¬H·“Ӧɜ³É £¬ŌņHĪŖ
£¬ŌņHĪŖ £®
£®
£Ø1£©·“Ó¦¢ŁŹĒ±½ŗĶ±ūĻ©·¢Éś¼Ó³É·“Ó¦£¬GĪŖCH2=C£ØCH3£©COCl£¬·Ö×ÓŹ½ĪŖ C4H5OCl£¬
¹Ź“š°øĪŖ£ŗ¼Ó³É·“Ó¦£»C4H5OCl£»
£Ø2£©AŹĒ £¬±½·ÓŗĶ¹żĮæÅØäåĖ®·¢ÉśČ”“ś·“Ó¦£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ
£¬±½·ÓŗĶ¹żĮæÅØäåĖ®·¢ÉśČ”“ś·“Ó¦£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø3£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬BµÄ½į¹¹¼ņŹ½ĪŖ£ŗ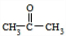 £¬ĘĖČČĻ¢Ķ“µÄ½į¹¹¼ņŹ½ĪŖ£ŗ
£¬ĘĖČČĻ¢Ķ“µÄ½į¹¹¼ņŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ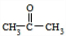 £»
£» £»
£»
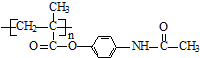
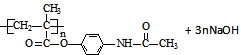
£Ø4£©ŗ¬ĘĖČČĻ¢Ķ“øß·Ö×ÓŅ©ĪļÓė×ćĮæĒāŃõ»ÆÄĘČÜŅŗ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ ”ś
”ś £¬
£¬
¹Ź“š°øĪŖ£ŗ ”ś
”ś £»
£»
£Ø5£©DĪŖCH2=C£ØCH3£©COOCH3£¬ĘäĶ¬·ÖŅģ¹¹ĢåŹōÓŚĮ“דõ„Ąą£¬ĒŅÄÜ·¢ÉśŅų¾µ·“Ó¦£¬Ó¦ĪŖ¼×ĖįŠĪ³ÉµÄõ„»ł£¬ŌņøĆĪļÖŹŹĒ¼×Ėįijõ„£¬ŠĪ³Éõ„µÄ“¼Ģ¼Į“½į¹¹ĪŖ£ŗC=C-C-C-”¢C-C=C-C-£ØÓŠĖ³·“£©”¢C-C-C=C-£ØÓŠĖ³·“£©”¢C=C£ØC£©-C-”¢C=C-C£ØC£©-”¢C-C£ØC£©=C-”¢C-C=C£ØC£©-£ØÓŠĖ³·“£©”¢C=C£ØC-C£©-£¬ĖłŅŌDµÄ·ūŗĻĢõ¼žµÄĶ¬·ÖŅģ¹¹ĢåÓŠ11ÖÖ£¬
¹Ź“š°øĪŖ£ŗ11£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄĶʶĻÓėŗĻ³É£¬Ć÷Č·ÓŠ»śĪļµÄ¹ŁÄÜĶż°ĘäŠŌÖŹŹĒ½ā±¾Ģā¹Ų¼ü£¬²ÉÓĆÕżÄęĻą½įŗĻµÄ·½·Ø½ųŠŠ·ÖĪö£¬ÄѵćŹĒĶ¬·ÖŅģ¹¹ĢåÖÖĄąµÄÅŠ¶Ļ£¬×¢ŅāÓŠĢ¼Į“Ņģ¹¹”¢¹ŁÄÜĶÅŅģ¹¹ŗĶĖ³·“Ņģ¹¹£¬ÄŃ¶Č½Ļ“ó£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Cu2+ H+ SO42- | B£® | Ba2+ NO3- CO32- | ||
| C£® | Al3+ H+ CO32- | D£® | OH- Cu2+ NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2H2+O2”ś2H2O+142.9kJ | B£® | 2H2£Øg£©+O2£Øg£©”ś2H2O£Øl£©+142.9kJ | ||
| C£® | 2H2£Øg£©+O2£Øg£©”ś2H2O£Øl£©+571.6kJ | D£® | H2O£Øl£©”śH2£Øg£©+$\frac{1}{2}$O2£Øg£©-142.9kJ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µā»Æ¼Ų | B£® | äåĖ® | C£® | µā¾Ę | D£® | µķ·Ū-KIČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ca£ØClO£©2ČÜŅŗÖŠĶØČėÉŁĮæSO2£ŗCa2++2ClO-+SO2+H2OØTCaSO3”ż+2HClO | |
| B£® | Ca£ØHCO3£©2ČÜŅŗÓėÉŁĮæNaOHČÜŅŗ·“Ó¦£ŗHCO${\;}_{3}^{-}$+OH-+Ca2+ØTCaCO3”ż+H2O | |
| C£® | C6H5ONaČÜŅŗÖŠĶØČėÉŁĮæCO2£ŗ2C6H5O-+CO2+H2O-”ś2C6H5OH+CO${\;}_{3}^{2-}$ | |
| D£® | ÓƶčŠŌµē¼«µē½āMgCl2ČÜŅŗ£ŗ2H2O+2Cl-$\frac{\underline{\;µē½ā\;}}{\;}$Cl2”ü+H2”ü+2OH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
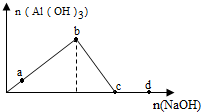
| A£® | aµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗK+”¢NH4+”¢I-”¢CO32- | |
| B£® | bµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗNa+”¢H+”¢S2-”¢Cl- | |
| C£® | cµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗNH4+”¢H+”¢NO3-”¢SO42- | |
| D£® | dµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗNa+”¢K+”¢SO42-”¢HCO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
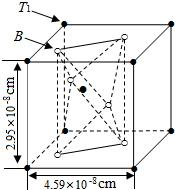
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Fe2+¾ßÓŠŃõ»ÆŠŌ£¬Ī¬ÉśĖŲC¾ßÓŠ»¹ŌŠŌ | |
| B£® | Fe2+¾ßÓŠŃõ»ÆŠŌ£¬Ī¬ÉśĖŲCŅ²¾ßÓŠŃõ»ÆŠŌ | |
| C£® | Fe2+¾ßÓŠ»¹ŌŠŌ£¬Ī¬ÉśĖŲC¾ßÓŠŃõ»ÆŠŌ | |
| D£® | Fe2+¾ßÓŠ»¹ŌŠŌ£¬Ī¬ÉśĖŲCŅ²¾ßÓŠ»¹ŌŠŌ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com