
【题目】下列说法中,正确的是( )
A.反应产物的总能量大于反应物的总能量时,△H<0
B.已知反应H2 (g)+I2(g)![]() 2HI(g)平衡常数为K,则2H2 (g)+2I2(g)
2HI(g)平衡常数为K,则2H2 (g)+2I2(g)![]() 4HI(g)的平衡常数为2K
4HI(g)的平衡常数为2K
C.ΔH<0、ΔS>0的反应在温度低时不能自发进行
D.在其他外界条件不变的情况下,使用催化剂,不能改变化学反应进行的方向
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.使酚酞变红色的溶液中:Na+、Al3+、SO42-、Cl-
B.![]() =1×10-13 mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
=1×10-13 mol·L-1的溶液中:NH4+、Ca2+、Cl-、NO3-
C.与Al反应能放出H2的溶液中:Fe2+、K+、NO3-、SO42-
D.水电离的c(H+)=1×10-13 mol·L-1的溶液中:K+、Na+、AlO2-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在溶液中可以大量共存的一组是( )
A.H+、Na+、OH﹣
B.Na+、NO3﹣、Cl﹣
C.K+、H+、HCO3﹣
D.Ca2+、SO42﹣、CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH滴定pH相同、体积相同的H2SO4、HCl、CH3COOH三种溶液,恰好中和时,所用相同浓度NaOH溶液的体积依次为V1、V2、V3,则这三者的关系是( )
A.V1>V2>V3 B.V1<V2<V3 C.V1=V2>V3 D.V1=V2<V3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】本世纪是生命科学研究的昌盛时期,科学家研究发现,进入生物体内的氧分子,可接受1个电子转变为超氧阴离子自由基(O2―),进而引发产生一系列自由基。一切需氧生物在其机体内均有一套完整的活性氧系统(抗氧化酶和抗氧化剂),能将活性氧转变为活性较低的物质,机体因此受到保护。人们利用羟胺(NH2OH)氧化的方法可以检测其生物系统中O2―含量,原理是O2―与羟胺反应生成NO2―和一种过氧化物。NO2―在对氨基苯磺酸和α—萘胺作用下,生成粉红的偶氮染料,该染料在λ=530nm处有显著吸收,且其吸收值与c(NO2―)成正比,从而可计算出样品中的O2―含量。某实验室用以上方法处理后测得溶液中:c(NO2―) =2.500×10-3 molL-1。
(1)请将测定原理有关的离子方程式缺少的物质补充完整并配平:
![]() NH2OH +
NH2OH +![]() O2― +
O2― +![]() H+=
H+=![]() NO2― +
NO2― +![]() +
+![]() H2O。
H2O。
(2)计算该样品中c(O2― ) = 。
(3)如用羟胺氧化法测定O2―时,将其生成的过氧化物作为检测物,若选用酸性K2Cr2O7溶液进行定量分析,请写出相应的离子方程式 。
(4)NO2―既有氧化性,又有还原性。NaNO2大量进入血液时,能将血红蛋白中的Fe2+氧化成Fe3+,正常的血红蛋白转化为高价铁血红蛋白,失去携氧功能,引起中毒,甚至死亡。下列各组试剂不能检验NO2―的是 。
A.FeCl2 KSCN B.KMnO4 H2SO4
C.AgNO3 HNO3 D.KI—淀粉试液
(5)某研究性学习小组,为研究光化学烟雾消长规律,在一烟雾实验箱中,测得烟雾的主要成分为RH(烃)、NO、NO2、O3、PAN(CH3COOONO2),各种物质的相对浓度随时间的消失,记录于右图,根据图中数据,请你判断下列推论中最不合理的是 。

A.NO的消失的速率比RH快 B.NO生成了NO2
C.RH及NO2可以生成PAN及O3 D.O3生成了PAN
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积一定的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g) + bB(g)![]() xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指( )
xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强)。在图中,Y轴是指( )

A.反应物A的百分含量
B.平衡混合气中物质B的百分含量
C.平衡混合气的密度
D.平衡混合气的平均摩尔质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2、CS2、COS是由C、O、S三种元素形成的结构相似的化合物。
(1)下列能说明碳、硫两种元素非金属性相对强弱的是 (填序号)
a.亚硫酸溶液加入Na2CO3溶液中,产生气泡
b.氧化性:浓H2SO4>H2CO3
c.CS2中碳元素为+4价,硫元素为﹣2价
d.SO2有较强还原性,而CO2无还原性
(2)羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害。
①羰基硫的结构式为: 。沸点:CO2_____COS(填“大于”或“小于” ),说明原因________。
②下列有关羰基硫的推测肯定不正确的是
A.COS分子中,所有原子都满足8电子的稳定结构
B.COS分子是含有极性键的非极性分子
C.COS分子中三个原子处于同一直线上
D.COS可能在O2中燃烧
③羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下图:

已知A是一种盐,则A的化学式为 ;气体单质a为 。
(3)在恒容密闭容器中,CO和H2S混合加热生成羰基硫的反应为CO(g)+H2S(g)![]() COS(g)+H2(g),反应前CO和H2S的物质的量均为10 mol,平衡后CO的物质的量为8 mol,回答下列问题:
COS(g)+H2(g),反应前CO和H2S的物质的量均为10 mol,平衡后CO的物质的量为8 mol,回答下列问题:
①升高温度,H2S浓度增加,表明该反应是___________________反应(填“放热”或“吸热”)。
②平衡时,继续通入CO 10 mol和H2S 10 mol,一段时间后再次达到平衡,此时H2S的转化率______(填“增大”“减小”“或”“不变“)。
(4)若反应在恒容密闭容器中进行,能说明该反应已达到平衡状态的是
a.容器内气体密度保持不变
b.CO、H2S、COS、H2的浓度均不再变化
c.c(H2)=c(H2S)
d.υ(H2)正=υ(H2S)逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可由乙苯生产苯乙烯: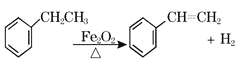 ,下列说法正确的是( )
,下列说法正确的是( )
A. 该反应的类型为消去反应
B. 乙苯的同分异构体共有三种
C. 可用Br2/CCl4鉴别乙苯和苯乙烯
D. 乙苯和苯乙烯分子内共平面的碳原子数均为7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com