
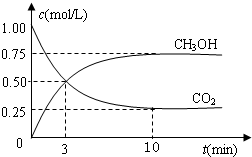
 �������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӣ� Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬��485��ʱ�������Ϊ1L���ܱ������У�����1mol CO2��3mol H2��һ�������·�����Ӧ�ϳɼ״���
�������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӣ� Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬��485��ʱ�������Ϊ1L���ܱ������У�����1mol CO2��3mol H2��һ�������·�����Ӧ�ϳɼ״���| ��c |
| ��t |
| n(CH3OH) |
| n(CO2) |
| 1.00mol/L-0.25mol/L |
| 10min |
| c(CH3OH)��c(H2O) |
| c(CO2)��c3(H2) |
| 0.75��0.75 |
| 0.25��0.753 |
| c(CH3OH)��c(H2O) |
| c(CO2)��c3(H2) |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£�23g NO2����NA����ԭ�� |
| B����״���£�22.4LCCl4����NA��CCl4���� |
| C��1molCH4�����к���2 NA����ԭ�� |
| D��0.5mol/L NaCl��Һ�к���0.5NA��Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Zn2++S2-+2H2O�TZn��OH��2��+H2S�� |
| B��Mg2++2HCO3-+2Ca2++4OH-�TMg��OH��2��+2CaCO3��+2H2O |
| C��FeS+2H+�TFe2++H2S�� |
| D��Cu2++H2S�TCuS��+2H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ����ʽ | ��Ӧ���� | ||
| ����������һ�ȴ��� | |||
| �ڱ�ϩͨ����ˮ�� | |||
| �۱�ϩ�Ӿ� | |||
| ��ʵ�����Ʊ���ϩ | |||
| �ݱ������� | |||
| �ޱ������ | |||
��CH3-CH=CH2+Cl2
|
|||
��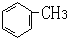
|
|||
��CH2=CHCH3
|
|||
| ��1-���������������ˮ��Һ | |||
| ?2-��������������Ƶ��Ҵ���Һ���� | |||
| ?�Ҵ�������Ʒ�Ӧ | |||
| ?�Ҵ������� | |||
| ?�����Ĵ����� | |||
| ?2-�����Ĵ����� | |||
| ?����������������Һ | |||
| ?���ӵμӵ���ˮ�� | |||
| ?��ȩ������������ͭ����Һ���� | |||
| ?��ȩ��������Һˮԡ���� | |||
| ?��ȩ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��4 | B��5 | C��6 | D��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2F2+2H2O=4HF+O2 |
| B��Cl2+H2O=HCl+HClO |
| C��SO2+O2=H2SO3 |
| D��2Na+H2O=2NaOH+H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��7.8g��Na2S��Na2O2��ɵĻ�����У����е���������Ϊ0.1NA |
| B��100g46%���Ҵ�ˮ��Һ�У����е���ԭ������Ϊ6NA |
| C���ھ���ͭ����ͭ�Ĺ����У�����������32gͭ��ת�Ƶ�����ΪNA |
| D��65gп��һ����Ũ����ǡ����ȫ��Ӧ����������ķ�����ΪNA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com