
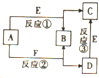
 物质A-F有如图所示的转化关系,已知B为非金属气态单质.
物质A-F有如图所示的转化关系,已知B为非金属气态单质.

 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
| A、将十水碳酸钠置于蒸发皿中,加热脱去结晶水 |
| B、用分液漏斗分离溴乙烷与氢氧化钠溶液发生反应后的生成物 |
| C、用铁粉与稀硝酸反应,制取少量氢气,用排水法收集 |
| D、用酸式滴定管量取6.55mL的KMnO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 现有A、B、C、D四种可溶性盐溶液,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别是NO3-、SO42-、Cl-、CO32-中的某一种.
现有A、B、C、D四种可溶性盐溶液,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别是NO3-、SO42-、Cl-、CO32-中的某一种.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 碳、氮、氧是构成生命物质的三种主要元素.
碳、氮、氧是构成生命物质的三种主要元素.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、放电时负极反应为:Zn-2e-+2OH-═Zn(OH)2 |
| B、充电时阳极反应为:Fe(OH)3-3e-+5OH-═FeO42-+4H2O |
| C、放电时正极产物是Zn(OH)2 |
| D、放电时正极附近溶液的碱性增强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com