
钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域。V2O5是接触法制硫酸的催化剂。
(1) 一定条件下,SO2 与空气反应t min后,SO2 和SO3 物质的量浓度分别为a mol/L、b mol·L-1,则SO2 起始物质的量浓度为_________mol/L ;生成SO3的化学反应速率为_____________________。
(2)全钒液流储能电池是利用不同价态离子对氧化还原反应来实现化学能和电能相互转化的,其装置原理如下图:
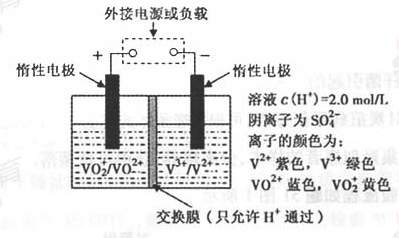
① 当左槽溶液逐渐由黄变蓝,其电极反应式为_______________________________。
② 充电过程中,右槽溶液颜色逐渐由__________色变为_______色。
③ 放电过程中氢离子的作用是________________和___________________________;充电时若转移的电子数为3.01×1023个,左槽溶液中n(H+)的变化量为______________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| b |
| t |
| b |
| t |

查看答案和解析>>
科目:高中化学 来源: 题型:
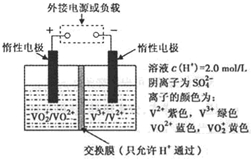 钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域.V2O5是接触法制硫酸的催化剂.
钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域.V2O5是接触法制硫酸的催化剂.| b |
| t |
| b |
| t |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| b |
| t |
| b |
| t |

查看答案和解析>>
科目:高中化学 来源:2010-2011学年四川成都外国语学校高三10月月考化学卷 题型:填空题
钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域。V2O5是接触法制硫酸的催化剂。
(1) 一定条件下,SO2 与空气反应t min后,SO2 和SO3 物质的量浓度分别为a mol/L、b mol·L-1,则SO2 起始物质的量浓度为_________mol/L ;生成SO3的化学反应速率为_____________________。
(2)全钒液流储能电池是利用不同价态离子对氧化还原反应来实现化学能和电能相互转化的,其装置原理如下图:
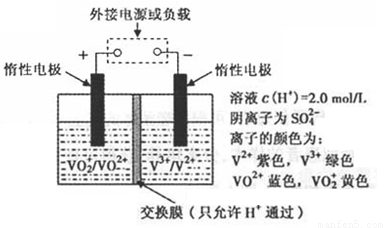
① 当左槽溶液逐渐由黄变蓝,其电极反应式为_______________________________。
② 充电过程中,右槽溶液颜色逐渐由__________色变为_______色。
③ 放电过程中氢离子的作用是________________和___________________________;充电时若转移的电子数为3.01×1023个,左槽溶液中n(H+)的变化量为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com