
| A. | 原子半径:Br>Se>Cl | B. | 热稳定性:HF>HCl>H2S | ||
| C. | 还原性:S2->Se2->Cl- | D. | 酸性:HBrO4>HClO4>H2SO4 |
分析 元素周期表中,同一周期元素从左到右,原子半径逐渐减小、非金属性逐渐增强,同主族自上而下,原子半径增大、元素的非金属性减弱,元素的非金属性越强,对应的氢化物越稳定,阴离子的还原性越弱,最高价氧化物对应的水化物的酸性越强,
A.同周期元素,原子半径随着原子序数增大而减小,同主族自上而下原子半径增大;
B.非金属的非金属性越强,其氢化物越稳定;
C.非金属的非金属性越强,其阴离子的还原性越弱;
D.非金属的非金属性越强,其最高价含氧酸的酸性越强.
解答 解:A.同周期元素从左到右,原子半径逐渐减小,同主族元素从上到下,原子半径逐渐增大,则应有Se>Br>Cl,故A错误;
B.非金属性F>Cl>S,元素的非金属性越强,对应的氢化物越稳定为:HF>HCl>H2S,故B正确;
C.非金属性Cl>S>Se,元素的非金属性越强,对应的阴离子的还原性越弱,则还原性Se2->S2->Cl-,故C错误;
D.非金属性Cl>Br>S,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则酸性HClO4>HBrO4>H2SO4,故D错误,
故选B.
点评 本题考查元素周期律知识,侧重于学生的分析应用能力的考查,注意把握同主族、同周期元素化合物的性质的相似性与递变性,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | SiO2$\stackrel{HCl}{→}$SiCl4$\stackrel{H_{2}}{→}$Si | |
| B. | MgCO3$\stackrel{HCl}{→}$MgCl2溶液$\stackrel{电解}{→}$Mg | |
| C. | Fe$→_{点燃}^{O_{2}}$Fe2O3$\stackrel{H_{2}SO_{4}}{→}$Fe2(SO4)3 | |
| D. | Na$→_{点燃}^{O_{2}}$Na2O2$\stackrel{CO_{2}}{→}$Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜片、石墨棒,乙醇 | B. | 铜片、石墨棒,硝酸银溶液 | ||
| C. | 锌片、铜片,稀盐酸 | D. | 铜片、铂片,FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸可以用于除去锅炉或水壶中的水垢 | |
| B. | 切开的苹果放置后变色和纸张久置后变黄的原理相同 | |
| C. | 蜂蚁蛰咬人时会向人体注入酸性物质,可涂抹小苏打溶液缓解疼痛 | |
| D. | 工业含酸废水可用氢氧化钡溶液处理后再排放,有利于减少水体污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数和中子数均为6的碳原子:${\;}_{6}^{6}$C | |
| B. | 硫离子的结构示意图: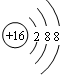 | |
| C. | 氢氧化钠的电子式: | |
| D. | 氮气分子的电子式: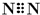 , , |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
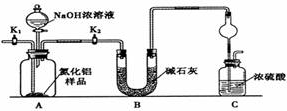
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
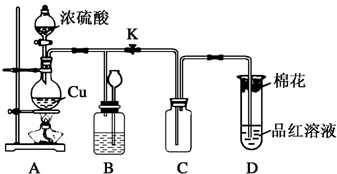
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
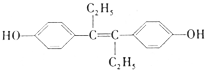
| A. | 可以用有机溶剂萃取 | |
| B. | 可与NaOH或NaHCO3溶液发生反应 | |
| C. | 1mol该有机物可以与5molBr2发生反应 | |
| D. | 该有机物分子中,可能有8个碳原子共平面 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com