
| 实验要求 | 所加试剂 | 主要操作 |
| 除去NaCl溶液中混有的I2 | 苯或四氯化碳 | 萃取、分液 |
| 除去NO气体中混有的NO2 | 水 | 洗气 |
| 除去SiO2固体中混有的Al2O3 | 盐酸 | 过滤 |
| 除去Fe2(SO4)3溶液混有的FeSO4溶液 | 过氧化氢 | ------ |
分析 碘不易溶于水,易溶于有机溶剂;
二氧化氮与水反应生成NO;
氧化铝与盐酸反应,而二氧化硅不能;
FeSO4溶液与过氧化氢反应生成硫酸铁.
解答 解:碘不易溶于水,易溶于有机溶剂,则除杂试剂为苯或四氯化碳,操作为萃取、分液;
二氧化氮与水反应生成NO,则除杂试剂为水,操作为洗气;
氧化铝与盐酸反应,而二氧化硅不能,则除杂试剂为盐酸,操作为过滤;
FeSO4溶液与过氧化氢反应生成硫酸铁,则除杂试剂为过氧化氢,
故答案为:
| 实验要求 | 所加试剂 | 主要操作 |
| 除去NaCl溶液中混有的I2 | 苯或四氯化碳 | 萃取、分液 |
| 除去NO气体中混有的NO2 | 水 | 洗气 |
| 除去SiO2固体中混有的Al2O3 | 盐酸 | 过滤 |
| 除去Fe2(SO4)3溶液混有的FeSO4溶液 | 过氧化氢 | ------ |
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及发生的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 把pH=2的甲酸溶液稀释100倍后pH=3.5 | |
| B. | 50mL l mol•L-1的甲酸溶液恰好与50mL l mol•L-1的NaOH溶液完全反应 | |
| C. | HCOONa溶液能使酚酞试液变红 | |
| D. | 0.1 mol•L-1的甲酸溶液的pH约为2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2使紫色石蕊溶液变红色:SO2+H2O═2H++SO32- | |
| B. | 在任何条件下都不能发生Cu+H2SO4═CuSO4+H2↑反应 | |
| C. | FeCl3、Na2O2、Cu2S均可由相应单质直接化合生成 | |
| D. | 浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气都首先发生置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KSCN溶液 | B. | NaOH溶液 | C. | 氨水 | D. | 石蕊试液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述过程中,最终被还原的是NO3- | |
| B. | 从上述过程中可以得出结论,氧化性:HNO3>稀H2SO4>Fe3+ | |
| C. | 上述过程中,会产生一种无色无味的难溶于水的气体 | |
| D. | 若通入的SO2完全反应,则同温同压下,SO2和逸出气体的体积为3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑥⑦ | B. | ②④⑥⑦ | C. | ④⑤⑥ | D. | ①③④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 阳离子 | K+、Ba2+、Fe2+、Al3+、Fe3+、Mg2+ |
| 阴离子 | OH-、HCO3-、CO32-、Cl-、NO3-、SO42- |
| A. | 由①、②判断,溶液中一定不含有的阳离子是K+、Fe3+ | |
| B. | 实验③中的气体不可能为CO2 | |
| C. | 综合分析判断,原溶液中所含的离子为:Fe2+、Mg2+、Cl-、NO3-、SO42- | |
| D. | 若向原溶液中加入足量的氢氧化钠溶液,充分反应后将沉淀过滤、灼烧至恒重,得到的固体质量为8g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
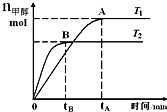 在恒容密闭的容器中,由CO合成甲醇:CO(g)+2H2(g)?CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )
在恒容密闭的容器中,由CO合成甲醇:CO(g)+2H2(g)?CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )| A. | 处于A点的反应体系从T1变到T2,达到平衡时$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$增大 | |
| B. | CO合成甲醇的反应为吸热反应 | |
| C. | 该反应在T1时的平衡常数比T2时的小 | |
| D. | 该反应平衡常数可表示为K=$\frac{c(C{H}_{3}OH)}{c(CO)c({H}_{2})}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
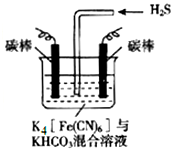 [Fe(CN)6]3-可将气态废弃物中的硫化氢转化为可利用的硫,自身还原为[Fe(CN)6]4-.工业上常采用如图所示的电解装置,通电电解,然后通入H2S加以处理.下列说法不正确的是( )
[Fe(CN)6]3-可将气态废弃物中的硫化氢转化为可利用的硫,自身还原为[Fe(CN)6]4-.工业上常采用如图所示的电解装置,通电电解,然后通入H2S加以处理.下列说法不正确的是( )| A. | 整个过程中需要不断补充K4[Fe(CN)6]与KHCO3 | |
| B. | 电解时阴极反应式为:2HCO3-+2 e-═H2↑+2CO32- | |
| C. | 当电解过程中有22.4L标准状况下的H2生成时,溶液中有32gS析出(溶解忽略不计) | |
| D. | 电解时阳极反应式为[Fe(CN)6]4--e-═[Fe(CN)6]3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com