


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源:不详 题型:单选题
| | 已知 | 类推 |
| A | 向次氯酸钙溶液中通CO2气体: Ca2++2ClO-+CO2+H2O =CaCO3↓+2HClO | 向次氯酸钙溶液中通SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HclO |
| B | 用惰性电极电解硫酸 铜溶液:2Cu2++2H2O 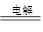 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ | 用铜电极电解硫酸铜溶液: 2Cu2++2H2O 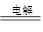 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
| C | 稀硫酸与Ba(OH)2溶 液反应,pH=7时, 2H++SO42—+Ba2++2OH- =BaSO4↓+2H2O | 硫酸氢钠溶液与Ba(OH)2溶液反应, pH=7时,2H++SO42—+Ba2++2OH- =BaSO4↓+2H2O |
| D | Ba(OH)2溶液逐滴滴入硫酸铝钾 溶液至沉淀质量达到最大值: 2Ba2++4OH-+Al3++2SO42— =2BaSO4↓+AlO2—+2H2O | Ba(OH)2溶液逐滴滴入硫酸铝铵溶液至沉淀 质量达到最大值: 2Ba2++4OH-+Al3++2SO42—=2BaSO4↓+ AlO2—+2H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向KI溶液中通入少量氯气:Cl2+2I-=2Cl-+I2 |
| B.向AlCl3溶液中滴入少量氨水:Al3++3OH-=Al(OH)3↓ |
| C.向NaHCO3溶液中滴入少量稀硫酸:2H++CO32-=CO2↑+H2O |
| D.向Fe2(SO4)3溶液中加入少量铁粉:Fe3++Fe=2Fe2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
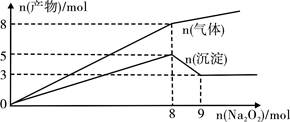
| A.2 mol、3 mol、8 mol |
| B.3 mol、2 mol、8 mol |
| C.2 mol、3 mol、4 mol |
| D.3 mol、2 mol、4 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.银离子 | B.亚铁离子 | C.镁离子 | D.铝离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
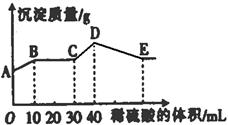
| A.AB段发生反应的离子方程式为:Ba2++SO42-=BaSO4↓ |
| B.E点对应横坐标稀硫酸的体积为70 ml |
| C.D点表示的沉淀的化学式为Al(OH)3、BaSO4 |
| D.E点沉淀比A点沉淀质量大2.33g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
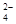 ,H2SO3,NH
,H2SO3,NH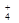 )分别进行如下实验:
)分别进行如下实验:| A.Br― | B.SO42- | C.H2SO3 | D.NH4+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液中c(SO42-)为0.1mol/L、c(CO32-) 为0.2mol/L |
| B.该混合物中不含Ba2+、Mg2+ |
| C.一定存在NH4+、 K+,无法确定Cl-是否存在 |
| D.实验(3)沉淀中加盐酸后,若只过滤、不洗涤,会对除NH4+外的其他离子含量的测定造成影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com