
【题目】制取一氯乙烷最好采用的方法是( )
A.乙烷与氯气反应B.乙烷与氯化氢反应
C.乙烯与氯气反应D.乙烯与氯化氢反应
科目:高中化学 来源: 题型:
【题目】山萘酚(Kaempf erol)结构如下图所示,且大量存在于水果、蔬菜、豆类、茶叶中,具有多种生物学作用,如抗氧化、抑制肿瘤生长及保护肝细胞等作用。下列有关山萘酚的叙述正确的是 ( )
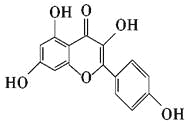
A. 结构式中含有羟基、醚键、酯基、碳碳双键
B. 可发生取代反应、水解反应、加成反应
C. 可与NaOH反应,不能与NaHCO3反应
D. 1 mol山萘酚与溴水反应最多可消耗4 mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ka (HCOOH)=1.77×10-4,Ka (CH3COOH)=1.75×10-5,Kb (NH3·H2O) =1.76×10-5,下列说法正确的是( )
A. 将CH3COONa溶液从20℃升温至30℃,溶液中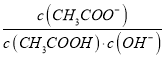 增大
增大
B. 用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等
C. 0.2 mol/L HCOOH 与 0.1 mol/L NaOH 等体积混合后:c(HCOO-) + c(OH-) = c(HCOOH) + c(H+)
D. 0.2 mol/L CH3COONa 与 0.1 mol/L盐酸等体积混合后 (pH<7):c(CH3COO-) > c(Cl- ) >c(CH3COOH) >c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
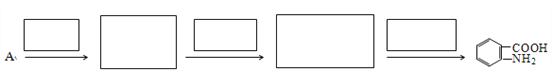
【题目】抗结肠炎药物有效成分M的合成路线如下(部分反应略去试剂和条件):
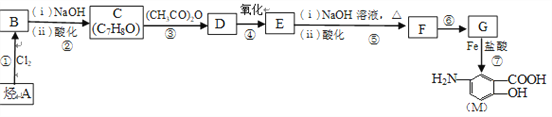
已知:
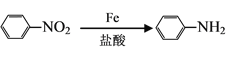
(1)烃A的结构简式是__________,G中的官能团名称是__________。
(2)反应①的反应条件是_________,反应⑥的反应类型是__________。
(3)下列对抗结肠炎药物有效成分M可能具有的性质推测正确的是________(填字母)。
A.既有酸性又有碱性 B.能发生消去反应
C.能发生加聚反应 D.1mol M与足量溴水充分反应,最多消耗1molBr2
(4)E与足量NaOH溶液反应的化学方程式是_______________________。
(5)写出符合下列条件的D的同分异构体的结构简式(任写一种)__________。
①属于芳香族化合物且苯环上有3个取代基
②能和NaHCO3溶液反应产生气体
③核磁共振氢谱有4组峰且峰面积之比为6∶2∶1∶1
(6)M在一定条件下可以发生缩聚反应生成含肽键的高分子化合物,写出该反应的化学方程式:_______________________________________________________
(7)已知:①![]() 易被氧化,②苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位。③苯环上连有羧基时再引入一个取代基,常取代在羧基的间位。参照以上的合成路线,设计一条以A为原料合成化合物
易被氧化,②苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位。③苯环上连有羧基时再引入一个取代基,常取代在羧基的间位。参照以上的合成路线,设计一条以A为原料合成化合物![]() 的合成路线。_______
的合成路线。_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是几种原子的基态电子排布,电负性最大的原子是
A. 1s22s22p4 B. 1s22s22p63s23p3 C. 1s22s22p63s23p2 D. 1s22s22p63s23p64s2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小分子抗癌药物的分子结构如图所示,下列说法正确的是

A. 1mol该有机物最多可以和5mol NaOH反应
B. 该有机物容易发生加成、取代、中和、消去等反应
C. 该有机物遇FeCl3溶液不变色,但可使酸性KMnO4溶液褪色
D. 1mol该有机物与浓溴水反应,最多消耗3mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学需要配制450 mL 0.5 mol·L-1的NaOH溶液。请回答下列问题:
(1)在实验过程中用到的玻璃仪器有:玻璃棒、量筒、烧杯、______________、胶头滴管、试剂瓶。
(2)用托盘天平称量时,应将NaOH放在________称量,称取的固体质量为_______。
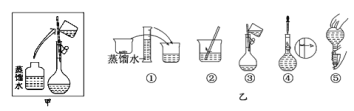
(3)配制时操作步骤如乙图所示,则甲图操作应在乙图中的___(填选项字母)之间。
A.①与② B.②与③ C.③与④ D.④与⑤
(4)配制过程中洗涤烧杯、玻璃棒2~3次的目的是______________________。
(5)定容滴加蒸馏水时,若不慎超过了刻度线,则处理的方法是______________。
(6)该同学实际配制NaOH溶液的浓度为0.6 mol·L-1,原因可能是____(填序号)。
a.砝码上有杂质
b.洗净的容量瓶中残留有少量水
c.称量NaOH固体时,采用了“左码右物”
d.定容时俯视刻度线
e.定容摇匀后发现液面低于刻度线又加入少许水调至刻度线
f.溶解固体的烧杯移液后未洗涤
g.定容前溶液未进行冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年,中科院大连化学物理研究所碳资源小分子与氢能利用创新特区研究组(DNL19T3)孙剑、葛庆杰研究员团队通过设计一种新型Na-Fe3O4/HZSM-5多功能复合催化剂,成功实现了CO2直接加氢制取高辛烷值汽油。该研究成果被评价为“CO2催化转化领域的突破性进展”。
(1) 工业生产尾气中的CO2捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至15.5~26.5℃后用氨水吸收过量的CO2,该反应的化学方程式为_____________。在用氨水吸收前,烟气需冷却至15.5~26.5℃的可能原因是_________________。
(2) 该研究成果用CO2制取高辛烷值汽油的路线是先将CO2按逆水煤气反应生成CO,然后由CO与H2反应生成烃,产物中汽油组分占所有烃类产物的百分比近80%。
① 已知:H2 (g)+![]() O2 (g) === H2O(l) ΔH1= —285.8 kJ·mol-1
O2 (g) === H2O(l) ΔH1= —285.8 kJ·mol-1
C8H18(l)+![]() O2(g) === 8CO2(g)+9H2O(l) ΔH3= —5518 kJ·mol-1
O2(g) === 8CO2(g)+9H2O(l) ΔH3= —5518 kJ·mol-1
试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方
程式__________________________。
② 在一实验容器中充入一定量的CO2和H2,若加入催化剂恰好完全反应,且产物只生成C5以上的烃类物质和水,则CO2与H2的物质的量之比不低于________。
(3) 二甲醚(CH3OCH3)的十六烷值高,燃烧尾气中污染物少,可代替柴油。CO、CO2混合加氢的方法是在一个反应器中将合成气直接转化为二甲醚,包括以下4个反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ①
CH3OH(g)+H2O(g) ①
CO2(g)+H2(g)![]() CO(g)+H2O(g) ②
CO(g)+H2O(g) ②
CO(g)+2H2(g)![]() CH3OH(g) ③
CH3OH(g) ③
2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ④
CH3OCH3(g)+H2O(g) ④
① 已知反应④在某温度下的平衡常数为K=400。此温度下,在一恒容密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
此时正、逆反应速率的大小:v(正) ______ v(逆) (填“>”、“<”或“=”)。
若加入CH3OH后,经10 min反应达到平衡,该时间内反应速率v(CH3OH)=_____。
② 某科研小组在反应温度503K~543K,反应压强分别是3、4、5、6、7MPa,n(CO)/n(CO+CO2)=0.5的情况下计算了二甲醚的平衡收率(二甲醚实际产量与反应物总量之比),结果如图1所示。

a~e曲线分别对应不同的压强条件,则e对应的压强是______,理由是___________。
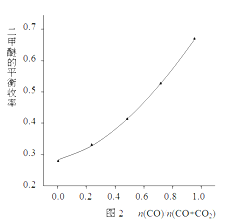
该科研小组在反应温度523K、反应压强5MPa的条件下,按照合成反应的化学计量比进料,改变n(CO)/n(CO+CO2)的比例,二甲醚的平衡收率的变化规律如图2所示。
由图2可知,二甲醚的平衡收率随着n(CO)/n(O+CO2)比值的增大而单调上升,其原因是________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,如图是海水综合利用的一个方面。

Ⅰ.(1)上述过程中没有涉及到的四大基本反应类型是 ______;
a.化合反应 b.分解反应 c.置换反应 d.复分解反应
(2)步骤1中分离操作的名称是___________;
(3)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:
a.盐酸 b.BaCl2溶液 c.NaOH溶液 d.Na2CO3溶液
加入试剂的顺序是_____________;
II.实验室利用精盐配制480mL 2.0mol·L1NaCl溶液。
(4)除容量瓶外,还需要的玻璃仪器有___________________;
(5)用托盘天平称取固体NaCl________g;
(6)配制时,按以下几个步骤进行:①计算 ②称量 ③溶解 ④冷却 ⑤转移 ⑥定容 ⑦摇匀 ⑧装瓶。操作中还缺少一个重要步骤是______________________;
(7)下列错误操作可使所配制氯化钠溶液浓度偏低的是(_________)
a.容量瓶洗净后残留了部分的水
b.转移时溶液溅到容量瓶外面
c.定容时俯视容量瓶的刻度线
d.摇匀后见液面下降,再加水至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com