
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:阅读理解
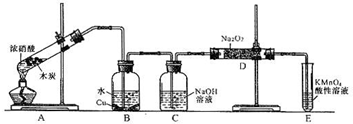
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热条件下均能与碳反应 | B、长期露置在空气中浓度均会升高 | C、常温下均不能用铁制容器贮存 | D、常温下均可与铜片迅速反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜和浓硫酸反应,亚硫酸钠和浓硫酸反应均可以制取二氧化硫 | B、铜和浓硝酸反应,碳和浓硝酸反应均可以制取二氧化氮 | C、向氯化铝溶液中加入过量氨水,或加入过量的氢氧化钠溶液均可制取氢氧化铝 | D、向次氯酸钙溶液中通入适量二氧化碳,或通入适量二氧化硫均可制取次氯酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
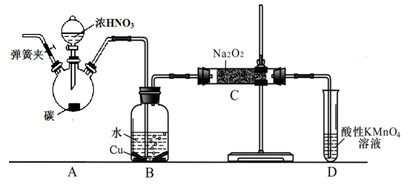
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com