
对于复分解反应:X+Y→Z+W,下列叙述正确的是( )
|
| A. | 若Z是强酸,则X和Y必有一种是强酸 |
|
| B. | 若X是强酸,Y是盐,反应后可能有强酸或弱酸生成 |
|
| C. | 若Y是强碱,X是盐,则Z或W必有一种是弱碱 |
|
| D. | 若W是弱碱,Z是盐,则X和Y必有一种是强碱 |
| 离子反应发生的条件. | |
| 专题: | 离子反应专题. |
| 分析: | A.有强酸生成的复分解反应中,反应物不一定有强酸,如H2S+CuSO4=CuS↓+H2SO4; B.反应物为强酸和盐,则反应产物中可能生成强酸或弱酸; C.反应物为强碱和盐,生成物中不一定有弱碱生成; D.反应物中有一种碱性强于W即可,反应物中不一定为强碱. |
| 解答: | 解:A.若Z是强酸,X和Y中可以都不是强酸,如:H2S+CuSO4=CuS↓+H2SO4,故A错误; B.若X是强酸,Y是盐,反应后可以生成强酸,如浓硫酸与氯化钠反应生成氯化氢和硫酸钠,也可以是弱酸,如盐酸与碳酸钠生成碳酸:Na2CO3+2HCl=2NaCl+CO2↑+H2O,故B正确; C.Y是强碱,X是盐,生成物Z和W可能都不是弱碱,如氢氧化钠与氯化铝的反应:AlCl3+4NaOH=NaAl(OH)4+3NaCl,反应生成两种盐,没有弱碱生成,故C错误; D.若W是弱碱,Z是盐,则X和Y中不一定有强碱,如:氨水与氯化铝反应生成氢氧化铝和氯化铵:AlCl3+3NH3•H2O=Al(OH)3↓+3NH4Cl,一水合氨为弱碱,故D错误; 故选B. |
| 点评: | 本题考查了复分解反应的判断,题目难度不大,注意掌握复分解反应概念及反应原理,对各选项判断时找出反例即可,试题培养了学生的分析、理解能力. |


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
有机物A是烃 ,有机物B易溶于水,且1 mol B能与足量的钠反应生成标准状况下的H2 11.2 L,
,有机物B易溶于水,且1 mol B能与足量的钠反应生成标准状况下的H2 11.2 L,
但不能与NaHCO3溶液反应,已知A通过如下转化关系(有关反应条件已略去)制得化学式为C4H8O2的酯E,且当D—→E时,相对分子质量增加28。
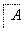
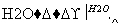
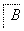
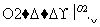
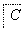
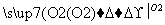
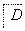
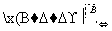

请回答下列问题:
(1)A的名称__________,结构简式__________________。
(2)A的官能团名称__________,B的官能团名称____________。
(3)反应①的反应类型为____________,反应③的反应类型为____________。
(4)4.4 g C物质完全燃烧消耗__________ mol氧气。
(5)完成下列反应的化学方程式:(有机物用结构简式表示)
反应②______________________________________________________________。
反应③______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列分类或归类正确的是( )
①铝热剂、纯净矿泉水、冰水混合物均为混合物
②NaOH、HD、IBr均为化合物
③明矾、烧碱、硫酸均为强电解质
④C60、金刚石、石墨均为碳的同素异形体
⑤碘酒、淀粉溶液、水雾、纳米材料均为胶体.
A.①②③④⑤ B. ③④⑤ C. ②④⑤ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液既能溶解Al(OH)3,又能溶解Al,但不能溶解Fe,在该溶液中可以大量共存的离子组是( )
|
| A. | K+、Na+、HCO | B. | Na+、SO |
|
| C. | NH | D. | H+、K+、Cl﹣、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
向等物质的量浓度的NaOH和Na2CO3的混合溶液中加入稀盐酸,下列离子方程式与事实不符的是( )
|
| A. | OH﹣+CO32﹣+2H+→HCO3﹣+H2O | B. | 2OH﹣+CO32﹣+3H+→HCO3﹣+2H2O |
|
| C. | 2OH﹣+CO32﹣+4H+→CO2↑+3H2O | D. | OH﹣+CO32﹣+3H+→CO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
某强碱性溶液中可能含有K+、NH4+、Al3+、AlO2﹣、SO42﹣、SiO32﹣、CO32﹣、Cl﹣中的某几种离子,现进行如下实验:
①取少量溶液用硝酸酸化后,加Ba(NO3)2溶液,无沉淀生成.
②另取少量溶液加入盐酸,其现象是:一段时间保持原样后,开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失.
(1)原溶液中肯定存在的离子是 肯定不存在的离子是
(2)已知一定量的原溶液中慢慢滴入5mL 0.2mol/L盐酸时,产生的沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g,则原溶液中是否含有Cl﹣?(通过列式说明) .
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用浓盐酸和MnO2共热制Cl2,并用Cl2和Ca(OH)2反应制少量漂白粉,现已知反应:
2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
温度稍高即发生副反应:6Cl2+6Ca(OH)2=Ca(ClO3)2 +5CaCl2+6H2O

现有三个同学分别设计的三套实验装置,如图所示:
(1)请从a.不容量控制反应速率;b.容量控制反应速率;c.有副反应发生;d.可防止副反应发生;e.污染环境;f.可防止污染环境等几个方面对上述甲、乙、丙三套装置的优缺点做出评析,并选择符合题目要求的选项填在空格内。
| 优点 | 缺点 | |
| 甲装置 | ||
| 乙装置 | ||
| 丙装置 |
(2)上述装置中,甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G两部分组成。请从上述装置中选取合理的组成部分,组装成一套较完善的实验装置,装置的各部分的连接顺序(按气流从左到右的方向)是 。
(3)实验中若用12mol·L-1的浓盐酸100mL与足量的MnO2反应,最终生成Ca(ClO)2的物质的量总是 0.15mol(填“大于”、“小于”或“等于”),其原因是(假定各步反应均无产物损耗,且无副反应发生) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除去杂质的方法正确的是 ( )
A.除去CO2中混有的CO:用澄清石灰水洗气
B.除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤
C.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤
D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com