
| A���������������mg����ʱ����������ͬʱ��mg�������� |
| B����ص�������ӦʽΪ��O2 + 2H2O + 4e���� 4OH�� |
| C������c(Na+)/c(CO32-) ��ֵ���䣬����ҺpH���ֲ��� |
| D�����һ��ʱ�䣬����ָ�Na2CO3ԭŨ�ȣ�ֻ��Ҫ����ˮ���� |
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
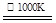 MnFe2O4��X��(X/2)O2
MnFe2O4��X��(X/2)O2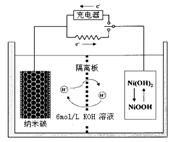
| ���� | H2 | CO | CH4 |
| ��ֵ/kJ��g�C1 | 143 | 10 | 56 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH + H2O)
CH3OH + H2O)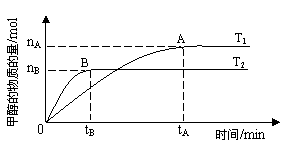
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��X������Y���� |
| B���õ�ع���ʱ��X��������Һ�ļ�����ǿ |
| C���ڱ�״���£�ͨ�� 5.6 L O2��ȫ��Ӧ����1 mol���ӷ���ת�� |
| D������һ��ʱ���KOH�����ʵ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������ڵ�����У�O2���ɸ��������� |
| B����ع���ʱ������1mol C4H10���ת��16mol e�� |
| C��ͨ�������һ�����������缫��ӦʽΪ��O2+4e��=2O2�� |
| D��ͨ�붡���һ��Ϊ�������缫��ӦʽΪ��C4H10+13O2��+26e��=4CO2+5H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���� | B���٢ڢ� | C���٢ڢ� | D���٢ڢۢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com