
分析 能导电的物质含有自由电子或自由离子,在水溶液里或熔融状态下能导电的化合物是电解质,能完全电离的电解质是强电解质,据此分析解答.
解答 解:①盐酸、②食盐水、⑥氨水是混合物,所以不是电解质,但都含自由离子所以能导电;
③熔化氯化钠是强电解质且含有自由移动的离子所以能导电;
④液态氯化氢是强电解质,但没有自由移动的离子,所以不导电;
⑤铜是单质所以不是电解质,但能导电;
⑦三氧化硫是非电解质,不能导电;
⑧醋酸是弱电解质,没有自由离子所以不导电;
可以导电并且属于强电解质的是③;
其中属于强电解质但是不导电的是④.
故答案为:③;④.
点评 本题考查了能导电的强电解质的判断,难度不大,紧扣“强电解质、能导电”来分析解答即可.


科目:高中化学 来源: 题型:填空题
 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:可能用到的有关数据如下:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:可能用到的有关数据如下:| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳酸钠一过氧化氢加合物(aNa2CO3•bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:
碳酸钠一过氧化氢加合物(aNa2CO3•bH2O2)具有漂白、杀菌作用.实验室用“醇析法”制备该物质的实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.5g | B. | 3g | C. | 6g | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
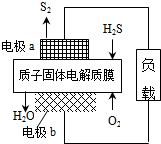 H2S废气资源化利用途径之一是回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.如图为质子膜H2S燃料电池的示意图.下列说法正确的是( )
H2S废气资源化利用途径之一是回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)═S2(s)+2H2O(l)△H=-632kJ•mol-1.如图为质子膜H2S燃料电池的示意图.下列说法正确的是( )| A. | 电极a为电池的正极 | |
| B. | 电极b上发生的电极反应为:O2+2H2O+4e-=4 OH- | |
| C. | 电路中每流过4mol电子,电池内部释放632kJ热能 | |
| D. | 每17gH2S参与反应,有1mol H+经质子膜进入正极区 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 颜色相似 | B. | 都是双原子分子 | ||
| C. | 最外层电子数相同,都是7 | D. | 自然界中都以化合态存在 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com