
| A、0.1mol |
| B、大于或等于0.2mol,小于0.3mol |
| C、0.2mol |
| D、大于0.1mol小于0.3mol |
| 8.96L |
| 22.4L/mol |
| 26.4g |
| 44g/mol |
| 0.6mol |
| 0.4mol |
| x+2y |
| x+y |
| 1 |
| 2 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 电石的主要成分为CaC2,易与水反应生成C2H2,故C2H2俗称电石气.某同学设计如下方案测定电石中CaC2的纯度(杂质不参加反应).
电石的主要成分为CaC2,易与水反应生成C2H2,故C2H2俗称电石气.某同学设计如下方案测定电石中CaC2的纯度(杂质不参加反应).查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 铁、铜、铝三种金属及其化合物在科学研究和工业生产中具有广泛用途.
铁、铜、铝三种金属及其化合物在科学研究和工业生产中具有广泛用途.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5(a+b) mol |
| B、(a-b) mol |
| C、0.5(a-b) mol |
| D、(a+b)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、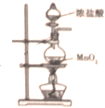 制取氯气的发生装置 |
B、 除去粗盐溶液中的难溶物 |
C、 蒸干氯化铝溶液制AlCl3?6H2O晶体 |
D、 除去氯气中的少量氯化氢 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com