
建构数学模型来研究化学问题,既直观又简洁。下列建构的数轴模型正确的是 ( )
A.钠在氧气中燃烧,钠的氧化产物: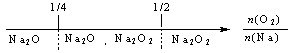
B.铁在Cl2中燃烧,铁的氧化产物: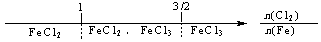 [来
[来
C.NH3与Cl2反应,反应产物: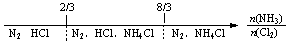
D.FeBr2溶液中通入Cl2,铁元素存在形式: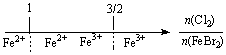
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
某无色溶液中只可能含有①Na+、②Ba2+、③Cl-、④Br-、⑤SO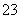 、⑥SO
、⑥SO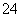 中的若干种(忽略水电离出的H+、OH-),依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
中的若干种(忽略水电离出的H+、OH-),依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
| 步骤 | 操作 | 现象 |
| (1) | 用pH试纸检验 | 溶液的pH大于7 |
| (2) | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈橙色 |
| (3) | 向所得水溶液中加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| (4) | 过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
下列结论正确的是
A.肯定含有的离子是③④⑤ B.肯定没有的离子是②⑤
C.可能含有的离子是①⑥ D.不能确定的离子是③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO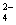 完全沉淀;如加入足量强碱并加热可得到c mol NH3,则原溶液中的Al3+浓度(mol·L-1)为( )
完全沉淀;如加入足量强碱并加热可得到c mol NH3,则原溶液中的Al3+浓度(mol·L-1)为( )
A.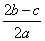 B.
B.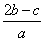 C.
C.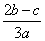 D.
D.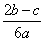
查看答案和解析>>
科目:高中化学 来源: 题型:
将15ml.2mol/LNa2CO3溶液逐滴加入到40 ml.0.5mol/LMCln盐溶液中,恰好将溶液中的Mn+离子完全沉淀为碳酸盐,则MCln中n值是 ( )
A.4 B.3 C.2 D.1
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数的值,下列叙述正确的是 ( )
A.标准状况下,4.0 g CH4中含有共价键的数目为NA
B.常温常压下,6.4 g氧气和臭氧中含有的分子总数为0.2NA
C. 0.3 mol·L-1的NH4NO3溶液中含有的NO3-数目为0.3NA
D.一定条件下6.4g SO2与足量氧气反应生成SO3,转移电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,下列叙述正确的是 ( )
A.pH=2的HA酸溶液与pH=12的MOH碱溶液以任意比混合:
c(H+) + c(M+)=c(OH-) + c(A-)
B.将物质的量浓度均为0.1mol·L−1的Na2CO3溶液、NaHCO3溶液等体积混合所得溶液中:2c(OH−)-2c(H+)=3c(H2CO3)+c(HCO3-)-c(CO32−)
C.等浓度、等体积的Na2CO3和NaHCO3混合: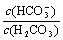 <
<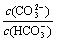
D.将足量AgCl分别放入:①5m水②10mL0.2mol/LMgC12③20mL0.3mol/L盐酸中溶解至饱和,c(Ag+):①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
我国部分城市灰霾天占全年一半,引起灰霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3,有机颗粒物及扬尘等。通过测定灰霾中锌等重金属的含量,可知目前造成我国灰霾天气主要是交通污染。
(1) Zn2+在基态时核外电子排布式为 ▲
(2) SO42-的空间构型是 ▲ (用文字描述)。
(3) PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾污染,光化学烟雾中含有NOX、O3, CH2=CH-CHO, HCOOH, CH3COOONO2(PAN)等二次污染物。
①下列说法正确的是 ▲ (不定项选择)。
a. N2O结构式可表示为N=N=O
b. O3分子呈直线形
c.CH2=CH-CHO分子中碳原子均采用sp2杂化
d.相同压强下,HCOOH沸点比CH30CH3高,说明前者是极性分子,后者是非极性分子
②1mo1PAN中含σ键数目为 ▲ 。
③NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]S04,该配合物中心离子的配位数为
 ▲ (填数字).
▲ (填数字).
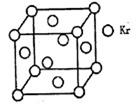
(4)测定大气中PM2.5的浓度方法之一是β一射线吸收法,β一射线放射源可用85Kr,已知Kr晶体的晶胞结构如图所示,设晶体中与每个Kr原子相紧邻的Kr原子有m个,晶胞中含Kr原子为n个,则m/n= ▲ (填数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
以石化产品乙烯、丙烯为原料合成厌氧胶的流程如图:

关于该过程的相关叙述正确的是( )
|
| A. | 反应④的反应类型是缩聚反应 |
|
| B. | 物质A是卤代烃 |
|
| C. | 物质B催化氧化后可以得到乙醛 |
|
| D. | 1 mol物质D最多可以消耗2 mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
磷酸铁(FePO4 ·2H2O,难溶于水的米白色固体)可用于生产药物、食品添加剂和锂离子电池的正极材料。
·2H2O,难溶于水的米白色固体)可用于生产药物、食品添加剂和锂离子电池的正极材料。
实验室可通过下列实验制备磷酸铁。
(1)称取一定量已除去油污的废铁屑,加入稍过量的稀硫酸,加热、搅拌,反应一段时间后过滤。反应加热的目的是_______________________。
(2)向滤液中加入一定量H2O2氧化Fe2+。为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+, 离子方程式如下:
离子方程式如下:
Cr2O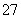 +6Fe2++14H+===2Cr3++6Fe3++7H2O
+6Fe2++14H+===2Cr3++6Fe3++7H2O
①在向滴定管中注入K2Cr2O7标准溶液前,滴定管需要检漏、________________________________和__________________________。
②若滴定x mL滤液中的Fe2+,消耗a mol·L-1 K2Cr2O7标准溶液b mL,则滤液中c(Fe2+)=________ mol·L-1。
③为使滤液中的Fe2+完全被H2O2氧化,下列实验条件控制正确的是________(填选项字母)。
A.加入适当过量的H2O2溶液
B.缓慢滴加H2O2溶液并搅拌
C.加热,使反应在较高温度下进行
D.用氨水调节溶液pH=7
(3)将一定量的Na2HPO4溶液(溶液显碱性)加入到含有Fe3+的溶液中,搅拌、过滤、洗涤、干燥得到FePO4·2H2O。若反应得到的FePO4·2H2O固体呈棕黄色,则磷酸铁中混有的杂质可能为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com