
| A. | 若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | |
| B. | 由“C(石墨)═C(金刚石)△H=1.9 kJ•mol”可知,金刚石比石墨稳定 | |
| C. | 在101 kPa时,2 g H2 完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol | |
| D. | 在稀溶液中:H++OH-═H2O△H=-57.3 kJ•mol,若将含1 mol H2SO4与含2 mol NaOH的溶液混合,放出的热量等于114.6 kJ |
分析 A.根据气体变成固体放热判断;
B.石墨能量比金刚石小,较稳定;
C.2gH2全燃烧生成液态水,放出285.8kJ热量,4gH2全燃烧生成液态水,放出517.6kJ热量;
D.1 mol H2SO4与含2 mol NaOH的溶液混合生成2mol水,以此计算放出的热量.
解答 解:A.固体硫变为硫蒸汽要吸热,则燃烧时放出的热量较少,故A错误;
B.反应为吸热反应,则石墨能量比金刚石小,能量越低越稳定,故B错误;
C.101 kPa时,2gH2 完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-517.6 kJ/mol,故C错误;
D.H++OH-═H2O△H=-57.3 kJ•mol,可知生成1mol水放出57.3kJ的热量,则1 mol H2SO4与含2 mol NaOH的溶液混合生成2mol水,放出的热量等于114.6 kJ,故D正确.
故选D.
点评 本题考查反应热与焓变,综合考查学生对化学反应与能量变化的理解,为高考常见题型,注意相关基础知识的积累,注意把握问题的角度,理解物质的聚集状态与能量的关系、稳定的大小比较等问题.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:选择题
| 时间/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
| A. | 反应在前50s的平均反应速率为v(PCl3)=0.0064 mol/(L•s) | |
| B. | 若保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol/L,则反应的△H<0 | |
| C. | 相同温度下,起始时向该容器中充入4.0 mol PCl3、4.0 mol Cl2,达到平衡时,PCl3的转化率小于80% | |
| D. | 相同温度下,起始时向该容器中充入2.0 mol PCl5、0.40 mol PCl3和0.40 mol Cl2,达到平衡前v(正)>v(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
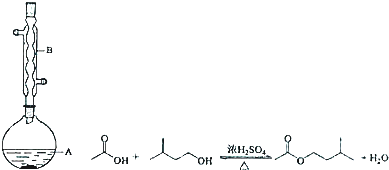
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戍醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验方案与步骤 | 实验现象和结论 |
| 1.将少量气体通入盛有少量品红溶液的试管内; | 若品红溶液褪色,则无色气体中有SO2. |
| 2.将气体通过装有足量氢氧化钠溶液的洗气瓶后,用小试管收集气体,并在酒精灯上点燃 | 若收集到气体可以燃烧,则无色气体中有H2. 结合以上实验可知假设三成立. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应都伴随着热量的变化 | |
| B. | 个别化学反应与能量变化无关 | |
| C. | 某些吸热反应在不加热条件下也能发生 | |
| D. | 放热反应的发生无需任何条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 编号 | ① | ② | ③ | ④ |
| 装置 | 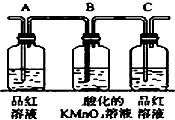 | 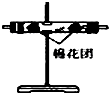 |  | 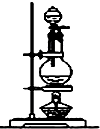 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | H-Cl | O═O | Cl-Cl | H-O |
| E/(kJ•mol-1) | 431 | 397 | a | 465 |
| A. | 242 | B. | 303.5 | C. | 180.5 | D. | 365 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 391 | B. | 194 | C. | 516 | D. | 658 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铜与硫酸溶液反应:Cu2++2H+═Cu2++H2O | |
| B. | 碳酸钠溶液与盐酸反应:Na2CO3+2H+═2Na++H2O+CO2↑ | |
| C. | 少量CO2通入澄清石灰水中:CO2+Ca2++2OH-═CaCO3↓+H2O | |
| D. | 钠投入到水中:Na+H2O═Na++OH-+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com