
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
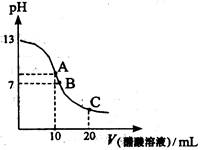
| A.在A点:c(Na+)> c(OH—)> c(CH3COO—)> c(H+) |
| B.在A点:c(Na+)+ c(H+)==c(OH—)+c(CH3COO—) |
| C.在B点:c(CH3COO—)> c(Na+)> c(H+)= c(OH—) |
| D.在C点:c(CH3COO—)> c(Na+)> c(H+)> c(OH—) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.14 | B.15 | C.16 | D.17 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 SO3(g)+NO(g)
SO3(g)+NO(g)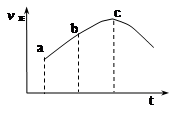
| A.反应物的总能量高于生成物的总能量 |
| B.反应物浓度:a点大于b点 |
| C.反应在c点达到平衡状态 |
| D.SO2的转化率:a点小于b点 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com