
| A. | H2D与H2T互为同素异形体 | |
| B. | 不同元素的原子构成的分子只含极性共价键 | |
| C. | ${\;}_{92}^{235}$U和${\;}_{92}^{238}$U是中子数不同、质子数相同的同种核素 | |
| D. | 短周期第 IVA与第 VIIA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
分析 A.同种元素形成的不同单质互为同素异形体;
B.H、O形成的化合物中能存在非极性共价键;
C.质子数相同,中子数不同的同种元素的不同核素互为同位素;
D.原子最外层电子数与其化合价绝对值之和为8,满足8电子结构.
解答 解:A.H2D与H2T为氢元素不同H原子形成的,结构相同为同一物质,故A错误;
B.H、O形成的化合物中能存在非极性共价键,如过氧化氢中存在极性键和非极性共价键,故B错误;
C.二者质子数相同,但是中子数不同,属于不同核素,互为同位素,故C错误;
D.短周期第IVA族与VIIA族元素的原子间构成的分子为AB4型,原子最外层电子数与其化合价绝对值之和均为8,满足8电子结构,故D正确;
故选:D.
点评 本题考查了同素异形体的概念,极性键和非极性共价键的判断等,题目难度不大,注意相关知识的积累.


科目:高中化学 来源: 题型:选择题
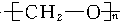 ,它是通过加聚反应制得的,则合成象牙的单体是( )
,它是通过加聚反应制得的,则合成象牙的单体是( )| A. | (CH3)2O | B. | CH3CHO | C. | HCHO | D. | C2H2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.18g | B. | 2.12g | C. | 4.22g | D. | 5.28g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
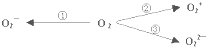 据2004年1月17日网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构,是一种高能量分子.
据2004年1月17日网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构,是一种高能量分子.
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 硫是氧化剂,KOH是还原剂 | |
| B. | 反应中共转移4摩尔电子 | |
| C. | 还原剂和氧化剂质量比是1:2 | |
| D. | 氧化产物和还原产物的质量比是1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酯的一般通式是RCOOR′和R′可以相同,也可以不同 | |
| B. | RCOOR′和R′可以是脂肪烃基,也可以是芳香烃基 | |
| C. | 在RCOOR′中,当R和R′均为-CH3时,这种酯叫甲酸甲酯 | |
| D. | 碳原子数相同的饱和一元羧酸和饱和一元酯互为同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com