

| A、分子式为C7H8O5 |
| B、能使溴的四氯化碳溶液褪色 |
| C、只能发生加成反应和取代反应 |
| D、分子中含有2种官能团 |
科目:高中化学 来源: 题型:
| A、若金属全部溶解,则溶液中一定含有Fe3+ |
| B、若金属有剩余,在溶液中再滴入硫酸后,金属不会开始溶解 |
| C、若金属全部溶解,且产生336mL气体(标准状况),则b=0.3 |
| D、当溶液中金属离子只有Fe3+、Cu2+时,则a与b关系为:b≥80y(1-a/3) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、实验甲:逐滴滴加盐酸时,开始无明显现象,然后才有大量气泡产生 |
| B、实验乙:充分振荡后静置,下层溶液为橙红色,上层无色 |
| C、实验丙:可测定胆矾晶体中结晶水的质量分数 |
| D、实验丁:酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅至褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、天然植物油常温下一般呈液态,难溶于水,有恒定的熔点、沸点 |
B、乙醛和丙烯醛( )不是同系物,它们与氢气充分反应后的产物也不是同系物 )不是同系物,它们与氢气充分反应后的产物也不是同系物 |
| C、若两种二肽互为同分异构体,则二者的水解产物不一致 |
| D、乙醛、氯乙烯和乙二醇均可作为合成聚合物的单体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | 乙烯使溴水褪色 苯使溴水褪色 | 均发生了加成反应 |
| B | 用pH试纸测定某盐酸的pH 用红色石蕊试纸检验某气体为氨气 | 试纸均需要蒸馏水湿润 |
| C | MnO2与浓盐酸反应制备Cl2 CaCO3与稀盐酸反应制备CO2 | 均发生氧化还原反应 |
| D | 淀粉在酶的作用下生成葡萄糖 蛋白质在酶的作用下生成氨基酸 | 均发生了水解反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、甲与乙互为同分异构体 |
| B、甲与乙都能与溴的四氯化碳溶液发生加成反应 |
| C、在一定条件下,甲与乙均能发生取代反应 |
| D、甲与乙都能与金属钠反应产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
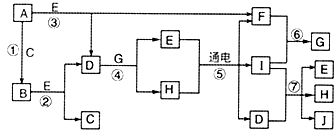 A-J是中学化学常见的几种物质,它们之间的转化关系如图所示.已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F合成,J可用作杀菌消毒剂.回答下列问题:
A-J是中学化学常见的几种物质,它们之间的转化关系如图所示.已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F合成,J可用作杀菌消毒剂.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com