
”¾ĢāÄæ”æ×¼Č·³ĘČ”6gĀĮĶĮæóѳʷ£Øŗ¬Al2O3”¢Fe2O3”¢SiO2£©£¬·ÅČė100mLÅØ¶ČµÄH2SO4ČÜŅŗÖŠ£¬³ä·Ö·“Ó¦ŗó¹żĀĖ£¬ĻņĀĖŅŗÖŠ¼ÓČė10mol/LµÄNaOHČÜŅŗ£¬²śÉś³ĮµķÓė¼ÓČėNaOHČÜŅŗµÄĢå»żµÄ¹ŲĻµČēÓŅĶ¼ĖłŹ¾£¬Ēó£ŗ
£Ø1£©ŌČÜŅŗÖŠc£ØH2SO4£©= mol/L
£Ø2£©Čōa=2.3mL£¬¼ĘĖćø÷×é·ÖµÄÖŹĮæ£ŗ
m£ØAl2O3£©= g£»m£ØFe2O3£©= g£»
£Ø3£©¼ĘĖćaÖµµÄȔֵ·¶Ī§£ŗ ””£¼a£¼ £®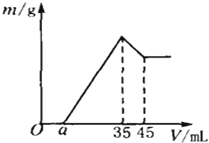
”¾“š°ø”æ1.75£»5.1£»0.72£»1.625£»5
”¾½āĪö”æ£Ø1£©µ±¼ÓČėNaOHČÜŅŗµÄĢå»żĪŖ35mlŹ±£¬n£ØNaOH£©=0.035L”Į10mol/L=0.35mol£¬
“ĖŹ±³ĮµķµÄÖŹĮæ“ļµ½×ī“óÖµ£¬Ōņ“ĖŹ±ČÜŅŗµÄČÜÖŹÖ»ÓŠNa2SO4 £¬
øł¾ŻNaŌŖĖŲŹŲŗćÓŠn£ØNa2SO4£©=![]() n£ØNaOH£©=
n£ØNaOH£©=![]() ”Į0.35mol=0.175mol£¬
”Į0.35mol=0.175mol£¬
øł¾ŻĮņĖįøłŹŲŗć£¬ŌņÓŠ£ŗn£ØH2SO4£©=0.175mol£¬
ĖłŅŌŌĮņĖįČÜŅŗÖŠc£ØH2SO4£©=![]() =1.75mol/L£¬
=1.75mol/L£¬
ĖłŅŌ“š°øŹĒ£ŗ1.75£»
£Ø2£©“Ó35mL”«45mL¼ÓČėµÄ10mLĒāŃõ»ÆÄĘĶźČ«ČܽāĒāŃõ»ÆĀĮ£¬øĆ½×¶ĪĻūŗĵÄn£ØNaOH£©=0.01L”Į10mol/L=0.1mol£¬øł¾Ż·½³ĢŹ½Al£ØOH£©3+NaOH=NaAlO2+2H2OæÉÖŖ£¬n[Al£ØOH£©3]=0.1mol£¬¹ŹČÜŅŗÖŠn£ØAl3+£©=0.1mol£¬øł¾ŻAlŌŖĖŲŹŲŗćæÉÖŖn£ØAl2O3£©=![]() ”Į0.1mol=0.05mol£¬Ōņm£ØAl2O3£©=0.05mol”Į102g/mol=5.1g£»
”Į0.1mol=0.05mol£¬Ōņm£ØAl2O3£©=0.05mol”Į102g/mol=5.1g£»
ĀĮĄė×ÓĶźČ«³ĮµķĻūŗÄĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæĪŖ0.1mol”Į3=0.3mol£¬ĢśĄė×Ó”¢ĀĮĄė×ÓĶźČ«³ĮµķĻūŗĵÄĒāŃõ»ÆÄĘČÜŅŗµÄĢå»żĪŖ35mL©2.3mL=32.7mL£¬¹ŹøĆ½×¶ĪĻūŗÄn£ØNaOH£©=0.0327L”Į10mol/L=0.327mol£¬¹ŹĢśĄė×ÓĶźČ«³ĮµķĻūŗĵÄĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæĪŖ0.327mol©0.3mol=0.027mol£¬¹Źn£ØFe3+£©=![]() =0.009mol£¬¹Źm£ØFe2O3£©=0.009mol”Į
=0.009mol£¬¹Źm£ØFe2O3£©=0.009mol”Į![]() ”Į160g/mol=0.72g£¬
”Į160g/mol=0.72g£¬
ĖłŅŌ“š°øŹĒ£ŗ5.1£»0.72£»
£Ø3£©ĀĮĄė×ÓĪļÖŹµÄĮæĪŖ0.1mol£¬ŅĄ¾Ż¼«Öµ·Ø¼ĘĖćaµÄ·¶Ī§£ŗÖ»ÓŠĀĮĄė×ÓŹ±³ĮµķŠčŅŖĒāŃõ»ÆÄĘĪļÖŹµÄĮæĪŖ0.3mol£¬ŠčŅŖĒāŃõ»ÆÄĘČÜŅŗĢå»żĪŖ30ml£¬Ōņa=35ml©30ml=5ml£¬µ«ŃłĘ·ÖŠŗ¬ÓŠŃõ»ÆĢś£¬aŅ»¶ØŠ”ÓŚ5ml£»¼ŁÉč6gijæóŹÆѳʷ֊ֻӊŗ¬Al2O3”¢Fe2O3 £¬ ŅĄ¾Ż£Ø2£©¼ĘĖćæÉÖŖm£ØAl2O3£©=5.1g£¬Ōņm£ØFe2O3£©=6g©5.1g=0.9g£¬n£ØFe2O3£©=![]() =0.005625mol£¬n£ØFe3+£©=0.005625mol”Į2=0.01125mol£¬ĻūŗÄĒāŃõøłĄė×Ó0.03375mol£»·“Ó¦ŠĪ³É×ī“óĮæ³ĮµķĻūŗÄĒāŃõ»ÆÄĘĪļÖŹµÄĮæĪŖ0.03375mol+0.3mol=0.33375mol£¬ŠčŅŖĒāŃõ»ÆÄĘČÜŅŗµÄĢå»żĪŖ
=0.005625mol£¬n£ØFe3+£©=0.005625mol”Į2=0.01125mol£¬ĻūŗÄĒāŃõøłĄė×Ó0.03375mol£»·“Ó¦ŠĪ³É×ī“óĮæ³ĮµķĻūŗÄĒāŃõ»ÆÄĘĪļÖŹµÄĮæĪŖ0.03375mol+0.3mol=0.33375mol£¬ŠčŅŖĒāŃõ»ÆÄĘČÜŅŗµÄĢå»żĪŖ![]() =0.033375L=33.375L£¬ĖłŅŌa×īŠ”ĪŖ35ml©33.375ml=1.625ml£»ŌņaµÄȔֵĪŖ£ŗ1.625£¼a£¼5£®
=0.033375L=33.375L£¬ĖłŅŌa×īŠ”ĪŖ35ml©33.375ml=1.625ml£»ŌņaµÄȔֵĪŖ£ŗ1.625£¼a£¼5£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ŹĒ²æ·Ö¶ĢÖÜĘŚŌŖĖŲŌ×Ó°ė¾¶ÓėŌ×ÓŠņŹżµÄ¹ŲĻµĶ¼”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
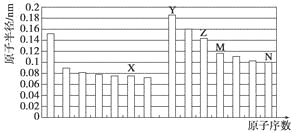
A. Z”¢NĮ½ÖÖŌŖĖŲµÄĄė×Ó°ė¾¶Ļą±Č£¬Ē°Õß½Ļ“ó
B. X”¢NĮ½ÖÖŌŖĖŲµÄĘųĢ¬Ēā»ÆĪļµÄ·ŠµćĻą±Č£¬Ē°Õß½ĻµĶ
C. ÓÉXÓėMĮ½ÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļ²»ÄÜÓėČĪŗĪĖį·“Ó¦£¬µ«ÄÜÓėĒæ¼ī·“Ó¦
D. ZµÄŃõ»ÆĪļÄÜ·Ö±šČܽāÓŚYµÄĒāŃõ»ÆĪļŗĶNµÄĒā»ÆĪļµÄĖ®ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ»śĪļGŹĒŅ»ÖÖ”°¦Ā©ŠĖ·Ü¼Į”±£¬ĘäŗĻ³ÉĀ·ĻßČēĻĀ£ŗ 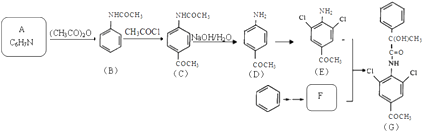 ŅŃÖŖ£ŗ
ŅŃÖŖ£ŗ 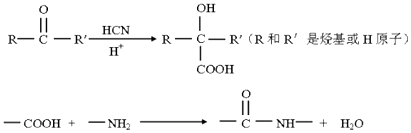
£Ø1£©Š“³ö»ÆŗĻĪļEĶ¬Ź±·ūŗĻĻĀĮŠĢõ¼žµÄĖłÓŠĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½
¢ŁŗģĶā¹āĘ×ĻŌŹ¾ŗ¬ÓŠČżÖÖ¹ŁÄÜĶÅ£¬ĘäÖŠĪŽŃõ¹ŁÄÜĶÅÓėEĻąĶ¬£¬²»ŗ¬¼×»ł
¢Ś1H©NMRĘ×ĻŌŹ¾·Ö×ÓÖŠŗ¬ÓŠ±½»·£¬ĒŅ±½»·ÉĻÖ»ÓŠŅ»ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒāŌ×Ó£®
¢Ū±½»·ÉĻÖ»ÓŠ4øöČ”“ś»ł£¬ÄÜ·¢ÉśŅų¾µ·“Ó¦
£Ø2£©ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A.»ÆŗĻĪļBÉś³ÉCµÄ·“Ó¦ĪŖČ”“ś·“Ó¦
B.1mol»ÆŗĻĪļD×ī¶ąÓė4molH2·¢Éś¼Ó³É·“Ó¦
C.»ÆŗĻĪļDÉś³ÉEµÄĢõ¼žĪŖÅØĀČĖ®/ĢśŠ¼
D.»ÆŗĻĪļGµÄ·Ö×ÓŹ½ĪŖC17H14Cl2NO3
£Ø3£©Š“³öE+F”śGµÄ»Æѧ·½³ĢŹ½
£Ø4£©øł¾ŻĢāÖŠŠÅĻ¢£¬Éč¼ĘŅŌ±½ŗĶCH3COClĪŖŌĮĻÖʱøFµÄŗĻ³ÉĀ·ĻߣØÓĆĮ÷³ĢĶ¼±ķŹ¾£¬ĘäĖūĪŽ»śŹŌ¼ĮČĪŃ”£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÓĆĶ¾²»ÕżČ·µÄŹĒ£Ø £©
A.ÓƶžŃõ»ÆĮņĘÆ°×Ņų¶śB.ÓĆĀČĘųÖʱøĘÆ°×·Ū
C.ÓĆŹ³ŃĪ×÷µ÷Ī¶¼ĮD.¹¤ŅµÉĻĄūÓƵŖĘųŗĻ³É°±
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķĮŠ³öĮĖ¢Ł”«¢āŹ®ÖÖŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆ£ŗ
¢ńA | ||||||||
1 | ¢Ł | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | |
2 | ¢Ś | ¢Ū | ¢Ü | |||||
3 | ¢Ż | ¢Ž | ¢ß | ¢ą | ¢į | ¢ā |
Ēė°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā”£
£Ø1£©ŌŖĖŲ¢ą¶ŌÓ¦µÄ¼ņµ„Ąė×ӵĽį¹¹Ź¾ŅāĶ¼ŹĒ____________”£
£Ø2£©ŅŌÉĻŌŖĖŲÖŠ£¬»ÆѧŠŌÖŹ×ī²»»īĘƵďĒ ____________£ØĢīŌŖĖŲ·ūŗÅ£©”£
£Ø3£©Š“³öŌŖĖŲ¢ŻŠĪ³ÉµÄµ„ÖŹŌŚæÕĘųÖŠČ¼ÉյĻÆѧ·½³ĢŹ½______________________£¬ÕāŅ»·“Ó¦ŹĒ____________(Ģī”°ĪüČČ”±»ņ”°·ÅČČ”±)·“Ó¦”£
£Ø4£©ÓƵē×ÓŹ½±ķŹ¾¢ÜÓė¢ŻŠĪ³ÉµÄA2BŠĶ»ÆŗĻĪļµÄŠĪ³É¹ż³Ģ___________________________”£
£Ø5£©ŌŚÕāŠ©ŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļÖŠ£¬ĖįŠŌ×īĒæµÄ»ÆŗĻĪļµÄ·Ö×ÓŹ½ŹĒ£ŗ__________£¬ÓėŌŖĖŲ¢ŽµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļ·¢Éś·“Ó¦Ź±µÄĄė×Ó·½³ĢŹ½ĪŖ________________
£Ø6£©¢ŪµÄ¼ņµ„Ēā»ÆĪļÓė¢ŪµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ·“Ó¦µÄÉś³ÉĪļÖŠŗ¬ÓŠµÄµÄ»Æѧ¼üÓŠ____________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ2016ÄźIUPACĆüĆū117ŗÅŌŖĖŲĪŖTs£ØÖŠĪÄĆū”° ![]() ”±£¬tiØ¢n£©£¬TsµÄŌ×ÓŗĖĶā×īĶā²ćµē×ÓŹżŹĒ7£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
”±£¬tiØ¢n£©£¬TsµÄŌ×ÓŗĖĶā×īĶā²ćµē×ÓŹżŹĒ7£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
A. TsŹĒµŚĘßÖÜĘŚµŚ¢÷A×åŌŖĖŲ B. TsµÄĶ¬Ī»ĖŲŌ×Ó¾ßÓŠĻąĶ¬µÄµē×ÓŹż
C. TsŌŚĶ¬×åŌŖĖŲÖŠ·Ē½šŹōŠŌ×īČõ D. ÖŠ×ÓŹżĪŖ176µÄTSŗĖĖŲ·ūŗÅŹĒ ![]() Ts
Ts
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼£¬ø÷ÉÕ±ÖŠŹ¢ÓŠŗ£Ė®£¬ĢśŌŚĘäÖŠ±»øÆŹ“µÄĖŁ¶ČÓÉæģµ½ĀżµÄĖ³ŠņĪŖ£Ø £© 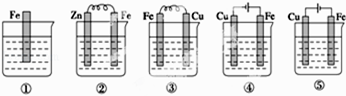
A.¢Ł¢Ś¢Ū¢Ü¢Ż
B.¢Ü¢Ū¢Ś¢Ł¢Ż
C.¢Ü¢Ū¢Ł¢Ś¢Ż
D.¢Ü¢Ś¢Ū¢Ł¢Ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ·“Ó¦KIO3+6HI=3I2+KI+3H2OÖŠ£¬Ńõ»Æ¼ĮÓė»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ
A. 1£ŗ1 B. 1£ŗ6 C. 1£ŗ5 D. 5£ŗ1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗ£Ė®ÖŠŗ¬ÓŠ·įø»µÄNa+”¢Mg2+”¢Cl©”¢Br©µČ»Æѧ׏Ō“£®½«ŗ£Ė®µ»ÆÓėÅØĖõŗ£Ė®½įŗĻŹĒ×ŪŗĻĄūÓĆŗ£Ė®×ŹŌ“µÄĶ¾¾¶Ö®Ņ»£®ŅŌÅØĖõŗ£Ė®ĪŖŌĮĻ£¬ĶعżŅ»ĻµĮŠ¹¤ŅÕĮ÷³ĢæÉŅŌĢįČ”Mg”¢Br2µČ²śĘ·£®
£Ø1£©ČēĶ¼ŹĒ²ÉÓĆĤ·ÖĄė¼¼ŹõµÄŗ£Ė®µ»ÆŹ¾ŅāĶ¼£®µ»ÆĤæÉŅŌČĆĖ®·Ö×ÓĶعż£¬¶ųŗ£Ė®ÖŠĘäĖū·Ö×ÓŗĶĄė×Ó¾ł²»ÄÜĶعż£®¼ÓŃ¹ŗó£¬×ó²ąµĖ®ÖŠŌö¼ÓµÄŹĒ£ØĢī×ÖÄø£©£® 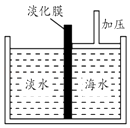
a£®ČÜÖŹÖŹĮæ b£®ČܼĮÖŹĮæ c£®ČÜÖŹµÄÖŹĮæ·ÖŹż
£Ø2£©“Óŗ£Ė®ÖŠĢįČ”Ć¾µÄÖ÷ŅŖ²½ÖčČēĻĀ£ŗ 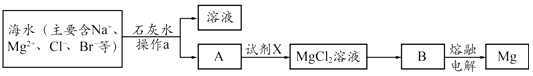
¢Ł²Ł×÷aµÄĆū³ĘŹĒ £®
¢ŚŠ“³öBŅ±Į¶½šŹōĆ¾µÄ»Æѧ·½³ĢŹ½ £®
£Ø3£©æÕĘų“µ³ö·ØŹĒÓĆÓŚ¹¤Ņµ¹ęÄ£ŗ£Ė®ĢįäåµÄ³£ÓĆ·½·Ø£¬ĘäÖŠŅ»ÖÖ¹¤ŅÕŹĒŅŌŌ¤ĻČ¾¹żĖį»ÆµÄÅØĖõŗ£Ė®ĪŖŌĮĻ£¬ĶعżŅŌĻĀ²½ÖčĢįČ”äå£ŗ ²½ÖčŅ»£ŗÓĆĀČĘųÖĆ»»äåĄė×ÓŹ¹Ö®³ÉĪŖµ„ÖŹä壻
²½Ö趞£ŗĶØČėæÕĘųŗĶĖ®ÕōĘų£¬½«ä哵ČėĪüŹÕĖž£¬Ź¹äåÕōĘųŗĶĪüŹÕ¼ĮSO2·¢Éś×÷ÓĆ×Ŗ»Æ³ÉĒāäåĖį£»
²½ÖčČż£ŗÓĆĀČĘų½«ĒāäåĖįŃõ»ÆµĆµ½²śĘ·ä壮
¢Ł²½ÖčŅ»ŗĶ²½Ö趞µÄÄæµÄŹĒ £®
¢Ś²½Ö趞֊·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com