
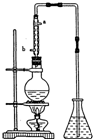
 市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\stackrel{{H}^{+}}{→}$ n(C2H4O)
市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\stackrel{{H}^{+}}{→}$ n(C2H4O)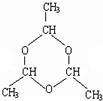 .
. 分析 本题是探究乙醛长期放置出现分层现象的原因,对混合物分离时涉及分液及蒸馏操作,考查了操作要点,如分层是用分液,混溶时用蒸馏,蒸馏时需要用冷凝管冷却,冷却水的流向为低进高出等,另外还考查了醛的化学性质如发生银镜反应及探究加合物的结构;
(1)久置的乙醛溶液会产生分层现象,因此分离时可选择分液漏斗通过分液进行操作;
(2)若乙醛被氧化,则生成CH3COOH,下层液呈酸性,可以利用石蕊试液检验下层液是否呈酸性;
(3)将少量乙醛溶液滴入热的浓硫酸中,有黑色固体物质生成,黑色物质为碳,浓硫酸具有强氧化性,可以氧化乙醛生成C,同时生成二氧化硫、水;
(4)蒸馏操作时会有部分加合物随温度的升高再挥发,如果不使用冷凝管使之液化后重新流入烧瓶内,会使得到的乙醛不纯,另外原料利用率也低;
(5)乙醛和银氨溶液在水浴加热的情况下,会生成光亮的银镜,同时自身被氧化成羧酸;
(6)乙醛分子间易形成化合物(C2H4O)n,醛基中羰基相互加成形成环状结构.
解答 解:(1)先分离混合物得到(C2H4O)n,基本方法是:将混合物放入分液漏斗中,静置分层后,打开活塞,将下层液体放入烧杯中,然后把上层的油状液体(C2H4O)n从分液漏斗的上口倒出,故答案为:分液;分液漏斗;
(2)若乙醛被氧化,则生成CH3COOH,下层液呈酸性,可以利用石蕊试液检验下层液是否呈酸性,具体操作为:取少量下层水溶液,滴加石蕊试液,如果溶液呈红色,说明部分乙醛已被氧化,故答案为:取少量下层水溶液,滴加石蕊试液,如果溶液呈红色,说明部分乙醛已被氧化;
(3)将少量乙醛溶液滴入热的浓硫酸中,有黑色固体物质生成,黑色物质为碳,浓硫酸具有强氧化性,可以氧化乙醛生成C,同时生成二氧化硫、水,反应方程式为:CH3CHO+H2SO4(浓)→2C↓+SO2↑+3H2O,故答案为:CH3CHO+H2SO4(浓)→2C↓+SO2↑+3H2O;
(4)利用冷凝管使挥发出的加合物液化后重新流入到烧瓶内,这样既保证了乙醛的纯度,也提高了原料的利用率,冷凝时冷却水的方向与蒸汽的流向相反,应该是低时高出,故答案为:使加合物冷凝回流到烧瓶内;b;
(5)乙醛发生银镜反应的化学方程式为CH3CHO+2Ag(NH3)2OH$\stackrel{加热}{→}$CH3COONH4+H2O+2Ag↓+2NH3,故答案为:CH3CHO+2Ag(NH3)2OH$\stackrel{加热}{→}$CH3COONH4+H2O+2Ag↓+2NH3;
(6)乙醛分子间易形成化合物(C2H4O)n,醛基中羰基相互加成形成环状结构,结构简式为: ,故答案为:
,故答案为: .
.
点评 本题考查了乙醛的化学性质,综合性较强,涉及混合物的分离和提纯、实验仪器、乙醛的特征反应等,难度一般.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
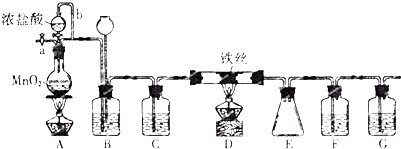
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
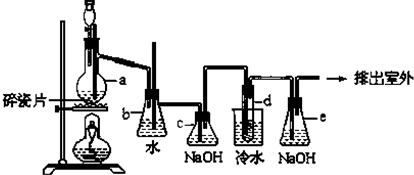
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间/s | 0 | 1 | 2 | 3 | 4 |
| c(SO2)/mol•L-1 | 1.00 | 0.50 | 0.23 | 3.00×10-37 | 3.00×10-37 |
| c(CO)/mol•L-1 | 4.00 | 3.00 | 2.46 | 2.00 | 2.00 |
| A. | 当v(SO2)正=2v(CO)逆时,该反应达到了平衡状态 | |
| B. | X的化学式为CO2 | |
| C. | 前1s内v(X)=1.00mol•L-1•s-1 | |
| D. | 上述反应达到平衡时,CO的转化率为50% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com