
下列中心原子的杂化轨道类型和分子几何构型不正确的是( )
A.CCl4中C原子sp3杂化,为正四面体形
B.BF3中B原子sp2杂化,为平面三角形
C.CS2中C原子sp1杂化,为直线形
D.H2S分子中,S为sp1杂化,为直线形
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年河南省五岳八校高二下期末联考化学试卷(解析版) 题型:选择题
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法不正确的是( )
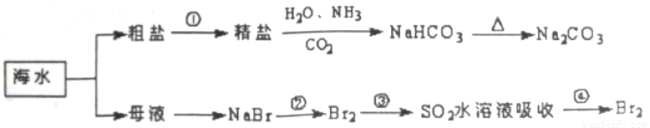
A.工业上通过电解熔融状态MgCl2制取金属镁
B.用澄清的石灰水可鉴别NaHCO3和Na2CO3
C.在第②、④步骤中,溴元素均被氧化
D.制取NaHCO3的反应是利用该条件下NaHCO3的溶解度小于NaCl
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省唐山市高二下期末化学试卷(解析版) 题型:推断题
【化学——选修3物质结构与性质】已知A、B、C、D、E、F是元素周期表中前36号元素,它们的原子序数依次增大。A的质子数、电子层数、最外层电子数均相等,B元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子总数相同,D的基态原子核外成对电子数是成单电子数的3倍,E是第四周期d区原子序数最大的元素,F+的最外层电子排布全充满。请回答下列问题:
(1)写出E的价层电子排布式 。
(2)A、B、C、D电负性由小到大的顺序为________(填元素符号)。
(3)E(BD)4为无色或黄色挥发性剧毒液体,熔点-19.3℃,沸点43℃。不溶于水,易溶于乙醇、乙醚、苯等有机溶剂,呈四面体构型,该晶体的类型为 ,E与BD之间的作用力为 。
(4)①写出一种与BD32-互为等电子体的分子的化学式 。
②含F2+的溶液与K2SO4、氨水反应可得到化合物 [F(NH3)4]SO4。1 mol配合物离子[F(NH3)4]2+中含σ键的数目为 。

③ E元素与镧(La)元素的合金可做储氢材料,该晶体的晶胞如图所示,晶胞中心有一个E原子,其他E原子都在晶胞面上,则该晶体的化学式为 ;已知该合金的摩尔质量为M g•mol-1,晶胞参数为a pm,用NA表示阿伏伽德罗常数,则该晶胞的密度为 g.cm-3。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省唐山市高二下期末化学试卷(解析版) 题型:选择题
下列说法正确的是
A.实验室制备Cl2,可用排饱和食盐水集气法收集
B.浓盐酸与KMnO4制氯气的离子方程式是:MnO4-+8H++2Cl- Mn2++Cl2↑+4H2O
Mn2++Cl2↑+4H2O
C.漂白粉溶液在空气中失效变化的离子方程式是:ClO-+CO2+H2O=HClO+HCO3-
D.H2O2具有很强的氧化性,在化学反应中只能作氧化剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省宁德市高二下期末化学试卷(解析版) 题型:选择题
据报道美国准备试验绿色航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,结构如图,它比肼燃烧释放能量更高,更安全、环保。下列说法不正确的是( )

A.羟基硝酸铵中各原子共平面
B.固态时羟基硝酸铵是离子晶体
C.羟基硝酸铵中含有离子键和共价键
D.9.6g羟基硝酸铵中含有0.2NA个离子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省宁德市高二下期末化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A.氯气通入氯化亚铁溶液中:Cl2+Fe2+=2Cl-+Fe3+
B.钠投入水中:Na+H2O=H2↑+Na++OH-
C.漂白粉的漂白原理:2ClO-+CO2+H2O=CO32-+2HClO
D.用小苏打治疗胃酸过多:HCO3-+H+=H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省周口市高二下期末化学试卷(解析版) 题型:填空题
【化学-选修3:物质结构与性质】
I .已知A、B、C、D、E、F为元素周期表中前四周期且原子序数依次增大的六种元素。其中A、B、C、D核电荷数之和为36, A、C原子的最外层电子数之和等于B原子的次外层电子数,D原子质子数为B原子质子数的两倍,E元素所在主族均为金属,F的价电子数 与C的核电荷数相等。
(1)下列关于上述几种元素的说法正确的是 。
a.B、C、D的原子半径由大到小的顺序为:D>C>B
B.E、F的最外层电子数相等
c.A、B、C、D四种元素中电负性和第一电离能最大的均为B
d.B与C形成的化合物中可能含有非极性键
e.A、C、F位于周期表的s区
(2)B单质有两种同素异形体。其中在水中溶解度较大的是 (填化学式),原因是 。
(3)EA2和A2B熔点较高的是 (填化学式),原因是 。
(4)D与B可以形成两种分子,其中DB2分子中心原子的杂化类型是 。
下列分子或离子中与DB3结构相似的是 。
a.NH3 B.SO32- C. NO3- D. PCl3
(5)已知B、F能形成两种化合物,其晶胞如图所示。则高温时甲易转化为乙的原因为 。
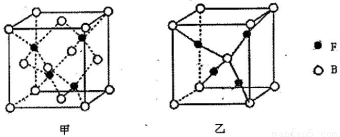
若乙晶体密度为pg/cm3,则乙晶胞的晶胞参数为a = nm。
Ⅱ.金属在化工生产及日常生活中有着广泛的应用,如铁、铬、镓等在现代工业中备受青睐。
(1)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态Cr原子中,未成对电子数有 个, Cr3+的价电子排布式为 。
(2) Zn与Ga的第一电离能从大到小的顺序为 。
(3)镓与第VA族元素可形成多种新型人工半导体材料, 砷化镓(GaAs)就是其中一种,其晶体结构如右图所示(白色球代表原子)。在GaAs晶体中,距离每个Ga原子最近的As原子有 个,距离每个As原子最近的As原子有 个。

(4)与As同主族的短周期元素是N、P,AsH3 空间构型为 ;一定压强下将AsH3和NH3、PH3的混合气体降温时首先液化的是 ,理由是 。
(5)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如下图所示,则氮化铁的化学为 ;设晶胞边长为acm,阿伏加德罗常数为 ,该晶体的密度为 g•cm-3(用含a和NA的式子表示)。
,该晶体的密度为 g•cm-3(用含a和NA的式子表示)。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省周口市高二下期末化学试卷(解析版) 题型:选择题
下列有关实验的做法正确的是 ( )
A. 用pH试纸测氯水的pH
B. 用托盘天平准确称取5.72 g NaCl晶体
C. 用酸式滴定管量取20.00 mL的酸性KMnO,溶液
D. 用带磨口玻璃塞的试剂瓶保存Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省宝鸡市岐山县高二下期末(有机)化学试卷(解析版) 题型:选择题
有8种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚丙烯;⑧环己烯。其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是( )
A.①②③⑤ B.①④⑥⑦ C.④⑥⑦⑧ D.②③⑤⑧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com