
| A. | 1.5 mol•L-1 | B. | 2 mol•L-1 | C. | 2.5 mol•L-1 | D. | 3 mol•L-1 |
分析 铁和氧化铁与硫酸反应后溶液中溶质为FeSO4、H2SO4,加入NaOH溶液使铁完全转化成Fe(OH)2,产生反应后的溶液溶质只有Na2SO4,根据硫酸根守恒,则n(H2SO4)=n(Na2SO4),根据钠离子守恒,则n(Na2SO4)=$\frac{1}{2}$n(NaOH),据此计算出原硫酸溶液中硫酸的物质的量,进而计算硫酸的物质的量浓度.
解答 解:铁和氧化铁与硫酸反应后溶液中溶质为FeSO4、H2SO4,加入NaOH溶液使铁完全转化成Fe(OH)2,反应后的溶液溶质只有Na2SO4,
根据硫酸根离子守恒可得:n(H2SO4)=n(Na2SO4),根据钠离子守恒可知:n(Na2SO4)=$\frac{1}{2}$n(NaOH)=$\frac{1}{2}$×3mol/L×0.2L=0.3mol,
所以原H2SO4的物质的量浓度为:c(H2SO4)=$\frac{0.3mol}{0.15L}$=2mol/L,
故选B.
点评 本题考查有关混合物反应的计算,题目难度中等,明确发生的反应原理为解题关键,注意利用守恒思想计算,侧重考查学生的分析思维能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 18个纵行代表18个族 | |
| B. | 短周期共有32种元素 | |
| C. | 元素周期表共有七个横行代表七个周期 | |
| D. | 第IA族全部是金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢能源代替化石能源 | B. | 推广使用太阳能电池 | ||
| C. | 电动汽车代替燃油汽车 | D. | 造纸厂污水直接排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,2molSO2和1molO2 混合在密闭容器中充分反应后容器中的分子数大于2NA | |
| B. | 256g S8分子中含S-S 键为7NA 个,12 克金刚石含C-C 键为4NA 个 | |
| C. | 由1molCH3COONa 和少量CH3COOH 形成的中性溶液中,CH3COO-数目为NA个 | |
| D. | 同温同压下,C18O 与N2的密度不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 吸收1638 kJ能量 | B. | 放出1638 kJ能量 | C. | 吸收126 kJ能量 | D. | 放出126 kJ能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
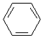 、④HCHO.其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是加成产物CH3OH分子之间能形成氢键.
、④HCHO.其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是加成产物CH3OH分子之间能形成氢键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{39}^{89}$Y的质子数与中子数之差为50 | |
| B. | ${\;}_{39}^{89}$Y和${\;}_{39}^{90}$Y互为同位素 | |
| C. | ${\;}_{39}^{89}$Y和${\;}_{39}^{90}$的核外电子数不相等 | |
| D. | ${\;}_{39}^{89}$Y和${\;}_{39}^{90}$是钇元素的两种不同的核素,具有不同的化学性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
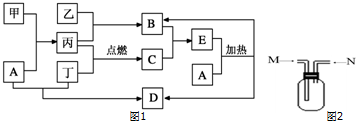
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com