
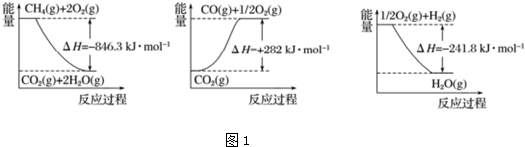
���� I��������ͼ���â�CH4��g��+2O2��g��=CO2��g��+2H2O��g����H=-846.3kJ•moL-1
��CO2��g���TCO��g��+$\frac{1}{2}$O2��g����H=+282kJ•moL-1
��$\frac{1}{2}$O2��g��+H2��g���TH2O��g����H=-241.8kJ•moL-1
��-�ۡ�3+�ڵ�CH4��g��+H2O��g��$\frac{\underline{\;����\;}}{\;}$CO��g��+3H2��g�����ʱ������Ӧ�ļ��㣻
II����1���ȼ��������̼��ƽ����Ӧ���ʣ��ٸ���ͬһ���淴Ӧ��ͬһʱ���ڸ����ʵķ�Ӧ���ʵ����������֮�ȼ�������ƽ����Ӧ���ʣ�A��˵���������¸�ʱ����������ʵ�Ũ����ȣ�
��ѧƽ�ⳣ��K����������Ũ����֮���뷴Ӧ����֮���ıȣ�
��2�������¶�ƽ�������ȷ����ƶ��������¶ȣ�ƽ������ȷ����ƶ���
��3���������ѹǿ��С��ƽ���������������ķ����ƶ���
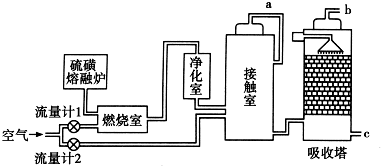
III����1����ԭ����У�ͨ���������ĵ缫��ʧ���ӷ���������Ӧ����ͨ���������ĵ缫�Ǹ�����ͨ��˫��ˮ�ĵ缫��������������˫��ˮ�õ�������ˮ��
��2��n��SO2��=$\frac{11.2L}{22.4L/mol}$=0.5mol������ת�Ƶ��Ӻ�ת��������֮��Ĺ�ϵʽ���㣮
��� �⣺��1��������ͼ���â�CH4��g��+2O2��g����CO2��g��+2H2O��g����H=-846.3kJ•moL-1
��CO2��g���TCO��g��+$\frac{1}{2}$O2��g����H=+282kJ•moL-1
��$\frac{1}{2}$O2��g��+H2��g���TH2O��g����H=-241.8kJ•moL-1
��-�ۡ�3+�ڵ�CH4��g��+H2O��g��$\frac{\underline{\;����\;}}{\;}$CO��g��+3H2��g����H=��-846.3+241.8��3+282��kJ•moL-1=+161.1kJ•moL-1���ʴ�Ϊ��+161.1kJ/mol��
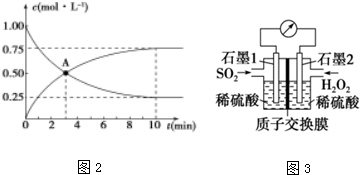
II����1��0��10min��v��CO2��=$\frac{1.00-0.25}{10}$ mol/��L��min��=0.075 mol/��L��min�����ٸ���ͬһ���淴Ӧ��ͬһʱ���ڸ����ʵķ�Ӧ���ʵ����������֮�ȵ�v��H2��=3v��CO2��=3��0.075 mol/��L��min��=0.225mol/��L��min����A��˵���������·�Ӧ3minʱ�������ʵ�Ũ����ȣ���c��CO2��=c��CH3OH����
��ѧƽ�ⳣ��K����������Ũ����֮���뷴Ӧ����֮���ıȣ���K=$\frac{c��C{H}_{3}OH����c��{H}_{2}O��}{c��C{O}_{2}����{c}^{3}��{H}_{2}��}$��
�ʴ�Ϊ��0.225mol/��L��min�����������·�Ӧ3minʱc��CO2��=c��CH3OH����$\frac{c��C{H}_{3}OH����c��{H}_{2}O��}{c��C{O}_{2}����{c}^{3}��{H}_{2}��}$��
��2���÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ���ı䷴Ӧ�¶�ΪT��CH3OH��Ũ����ÿ����0.030mol/L������˵��ƽ�������ƶ����¶�Ҫ����500�棬
�ʴ�Ϊ�������ı��¶ȣ��״���Ũ������˵��ƽ�������ƶ�����Ϊ�÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ����T��500�棻
��3���÷�Ӧǰ�����������С���������ѹǿ��С��ƽ���������������ķ����ƶ����������ƶ���
�ʴ�Ϊ���棻�÷�Ӧ���淴Ӧ���������������ķ�Ӧ�����������ݻ����൱�ڼ�Сѹǿ��ƽ�����������������ķ����ƶ���
III����1����ԭ����У�ͨ���������ĵ缫��ʧ���ӷ���������Ӧ����ͨ���������ĵ缫�Ǹ�����ͨ��˫��ˮ�ĵ缫��������������˫��ˮ�õ�������ˮ���缫��ӦʽΪH2O2+2e-+2H+=2H2O��
�ʴ�Ϊ��������H2O2+2e-+2H+=2H2O��
��2��n��SO2��=$\frac{11.2L}{22.4L/mol}$=0.5mol���÷�Ӧ�ĸ�����ӦʽΪSO2+2H2O-2e-=SO42-+4H+�������缫��ӦʽΪH2O2+2e-+2H+=2H2O����0.5mol��������μӷ�Ӧ����2mol�������������Ϸ�����Ӧ����Ǩ��H+�����ʵ���Ϊ��Ӧ�Ķ��������2����Ϊ1mol��
�ʴ�Ϊ��1mol��
���� �����漰��ѧƽ����㡢��Ӧ�ȼ��㡢ԭ���ԭ����֪ʶ�㣬Ϊ��Ƶ���㣬���ؿ���ѧ���������㼰֪ʶ�ۺ�������������ȷ��������Ի�ѧƽ��Ӱ�켰�缫��Ӧʽ����д�����ǽⱾ��ؼ�����д�缫��ӦʽҪ��ϵ������Һ����ԣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��Mg2+��Cl-��I- | B�� | Fe2+��Ba2+��S2-��Cl- | ||
| C�� | Na+��Al3+��Cl-��HCO3- | D�� | K+��Fe2+��Cl-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��FeCl2��Һ��ͨ��Cl2��Ӧ����FeCl3��Һ��Fe2++Cl2�TFe3++2Cl- | |
| B�� | CO2ͨ�������NaOH��Һ��CO2+OH-�THCO3- | |
| C�� | ����ʯ�������CaCO3+2H+�TCa2++CO2��+H2O | |
| D�� | ̼�ᱵ��ϡ���BaCO3+2H+�TBa2++CO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2 4 3 2 2 6 | B�� | 0 2 1 0 1 2 | ||
| C�� | 2 0 1 2 0 2 | D�� | 2 2 2 2 1 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
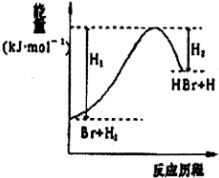
| A�� | �÷�ӦΪ���淴Ӧ | B�� | ��������������HBr�IJ��� | ||
| C�� | ��Ӧ������������������������ | D�� | ��Ӧ���ܼ��ܵ����������ܼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 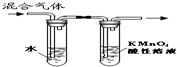 װ�ÿ����ڼ�����������ȥ��Ӧ�IJ��� | |
| B�� | 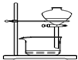 װ�ÿ����ڷų�������Ȼ�̼��Һ | |
| C�� | 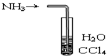 װ�ÿ���������NH3��ֹ���� | |
| D�� | 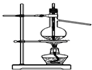 װ�ÿ�����ʵ�����Ʊ�����ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CaCO3��BaSO4��Na2CO3 | B�� | CuSO4��NaCl��NaCO3 | ||
| C�� | NaCl��CuSO4��CaCO3 | D�� | NaCl��KNO3��BaCl2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com