
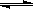 H++OH- KW=10-14 CH3COOH
H++OH- KW=10-14 CH3COOH 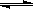 H++ CH3COO- Ka=1.8×10-5
H++ CH3COO- Ka=1.8×10-5| A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol·L-1 |
| B.若V1=V2,反应后溶液pH一定等于7 |
| C.若反应后溶液呈酸性,则V1一定大于V2 |
| D.若反应后溶液呈碱性,则V1一定小于V2 |
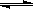 CH3COOH+OH-;增大(3)小于;大于(4)c(Na+)>c(CH3COO-)>c(OH-)>c(H+)(5)小于(6)BC(7)Cd2+、Zn2+;[OH-]=2.2×10-5mol·L-1 [M2+][OH-]2=5×10-12(mol·L-1)35×10-12小于KSP[Mg(OH)2]=1.8×10-115×10-12大于KSP[Zn(OH)2]=1.2×10-175×10-12大于KSP[Cd(OH)2]=2.5×10-14(8)1×10-12
CH3COOH+OH-;增大(3)小于;大于(4)c(Na+)>c(CH3COO-)>c(OH-)>c(H+)(5)小于(6)BC(7)Cd2+、Zn2+;[OH-]=2.2×10-5mol·L-1 [M2+][OH-]2=5×10-12(mol·L-1)35×10-12小于KSP[Mg(OH)2]=1.8×10-115×10-12大于KSP[Zn(OH)2]=1.2×10-175×10-12大于KSP[Cd(OH)2]=2.5×10-14(8)1×10-12 

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.Na+、Cu2+、SO42—、NH3·H2O |
| B.K+、Al3+、MnO4—、C2H5OH |
| C.K+、Cl—、NO3—、Fe2+ |
| D.Na+、NH4+、CH3COOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=13的溶液中:Na+、CO32―、Al3+、ClO― |
| B.c(H+)/c(OH―) =1010的溶液中:K+、Fe2+、Cl―、SO42― |
| C.加入铝片能放出H2的溶液中:Na+、HCO3―、Cu2+、SO42― |
| D.水电离出来的c(H+)=10-13mol·L-1的溶液中:NH4+、K+、NO3―、SiO32― |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe2+、Na+、Cl―、NO3― | B.Ba2+、Al3+、Cl―、NO3― |
| C.K+、Na+、HCO3―、Cl― | D.AlO2-、K+、OH―、Cl― |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、I- |
| B.pH值为1的溶液:Cu2+、Na+、Mg2+、NO3- |
| C.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ |
| D.所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.Na+、Al3+、Cl-、 | B.Cu2+、Cl-、 、OH- 、OH- |
C.Ca2+、Na+、 、 、 | D.H+、 、 、 、OH- 、OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.0mol/L的KNO3溶液:H+,Fe2+ ,K+,SO42- |
| B.与铝反应放出氢气的溶液:Na+,CH3COO-,HCO3-,SO42- |
| C.加入甲基橙试液呈红色的溶液:NH4+,K+,SO42-,Cl- |
| D.饱和氯水中:NO3-,Na+,SO32-,Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com