
| A. | NO2通FeSO4溶液中 | B. | NH3通入AlC13溶液中 | ||
| C. | CO2通入CaC12溶液中 | D. | SO2通人已酸化的Ba(NO3)2溶液中 |
分析 A.NO2和水反应生成NO和硝酸,硝酸可氧化FeSO4;
B.氨气水溶液呈碱性,可与氯化铝反应生成白色沉淀;
C.二氧化碳与氯化钙溶液不反应;
D.二氧化硫在酸化的硝酸钡溶液中被稀硝酸氧化生成硫酸钡沉淀分析.
解答 解:A.NO2和水反应生成NO和硝酸,硝酸具有强氧化性,可氧化FeSO4生成Fe3+,可观察到红棕色气体变为无色,溶液由浅绿色变成黄色,故A不选;
B.氨气水溶液呈碱性,可与氯化铝反应生成白色沉淀,故B不选;
C.二氧化碳与氯化钙溶液不反应,不能观察到明显现象,故C选;
D.二氧化硫在酸化的硝酸钡溶液中被稀硝酸氧化为硫酸,硫酸根离子结合钡离子生成硫酸钡沉淀,故D不选;
故选C.
点评 本题考查较为综合,涉及二氧化氮、氨气、二氧化硫以及沉淀的转化等知识,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,难度不大.


科目:高中化学 来源: 题型:解答题
| 粒子代码 | a | b | c | d | e | f | g |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 单位电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚与碳酸钠反应:2C6H5OH+CO32-→2C6H5O-+CO2↑+H2O | |
| B. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| C. | Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-═2Fe2++I2+3H2O | |
| D. | SO2通入溴水中:SO2+2H2O+Br2═2H++SO42-+2HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2和Cl2 | B. | Cu和 Cl2 | C. | H2和O2 | D. | Cu和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
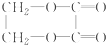 )所经历的反应的正确顺序是( )
)所经历的反应的正确顺序是( )| A. | ①⑤②③④ | B. | ①②③⑤④ | C. | ②③⑤①④ | D. | ②③⑤①⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制的氯水在光照下颜色变浅 | |
| B. | H2、I2、HI平衡混合气减小压强(扩大体积)可使颜色变浅 | |
| C. | 打开汽水瓶盖,有气泡冒出 | |
| D. | 在合成氨的反应中,加压有利于氨的合成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH→CH3COOC2H5 | B. | C2H5Cl→CH2=CH2 | ||
| C. | 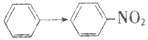 | D. | CH3CHO→C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
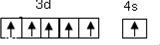
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| P>S | O2->Na+ | CaO<MgO | HClO4>H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com