
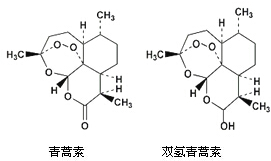
 中国女药学家屠呦呦因创新性抗疟药青蒿素和双氢青蒿素而获得诺贝尔生理学或医学奖.颁奖理由是“因为发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.下列关于青蒿素和双氢青蒿素(结构如图)说法错误的是( )
中国女药学家屠呦呦因创新性抗疟药青蒿素和双氢青蒿素而获得诺贝尔生理学或医学奖.颁奖理由是“因为发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”.下列关于青蒿素和双氢青蒿素(结构如图)说法错误的是( )| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 由青蒿素制备双氢青蒿素的反应属还原反应 | |
| C. | 青蒿素和双氢青蒿素均能跟氢氧化钠反应 | |
| D. | 青蒿素分子中含有过氧键和酯基、醚键 |
分析 A.根据结构简式确定分子式,交点为碳原子,用H原子饱和碳的四价结构;
B.青蒿素中酯基中羰基与氢气发生加成反应生成双氢青蒿素;
C.青蒿素中含有酯基,能与氢氧化钠反应,双氢青蒿素不能跟氢氧化钠反应
D.由青蒿素的结构简式,可知含有过氧键、酯基、醚键.
解答 解:A.由结构简式可知青蒿素的分子式为C15H22O5,故A正确;
B.青蒿素与氢气发生加成反应生成双氢青蒿素,属于还原反应,故B正确;
C.青蒿素中含有酯基,能与氢氧化钠反应,双氢青蒿素含有羟基、醚键、过氧键,不能跟氢氧化钠反应,故C错误;
D.由青蒿素的结构简式,可知含有过氧键、酯基、醚键,故D正确.
故选:C.
点评 本题考查有机物的结构与性质,注意掌握官能团结构与性质,是有机化学常考题型,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
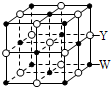 X、Y、Z、Q、R、W是原子序数依次增大的前四周期元素.X的原子核内无中子,Y与Z能形成两种无色无味的气体,Q与X同族,R在同周期主族元素中原子半径最小,基态原子W的3d能级有2个空轨道.请回答下列问题:
X、Y、Z、Q、R、W是原子序数依次增大的前四周期元素.X的原子核内无中子,Y与Z能形成两种无色无味的气体,Q与X同族,R在同周期主族元素中原子半径最小,基态原子W的3d能级有2个空轨道.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO | B. | NH3 | C. | H2O2 | D. | CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
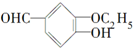 ,下列对该物质叙述正确的是( )
,下列对该物质叙述正确的是( )| A. | 该物质可以进行消去反应 | |
| B. | 该物质可以进行水解反应 | |
| C. | 1 mol该物质最多可与3 mol H2反应 | |
| D. | 该物质可以和Br2进行取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水,S${O}_{3}^{2-}$浓度增大 | |
| B. | 通入少量Cl2气体,溶液pH增大 | |
| C. | 加少量CaSO3粉末,HS${O}_{3}^{-}$ 浓度基本不变 | |
| D. | 通入少量HCl气体,溶液中HS${O}_{3}^{-}$ 浓度减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氧化剂H2O2在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注.
氧化剂H2O2在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注.| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL 2%H2O2溶液 | 无 |
| ② | 10mL 5%H2O2溶液 | 无 |
| ③ | 10mL 5%H2O2溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ④ | 10mL 5%H2O2溶液+少量HCl溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL 5%H2O2溶液+少量NaOH溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
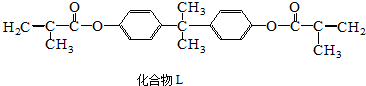
| A. | 1mol L分别与足量NaOH溶液和H2反应,最多可消耗4molNaOH和10molH2 | |
| B. | 有机酸M与油酸互为同系物,双酚A与苯酚互为同系物 | |
| C. | 与M含相同官能团的同分异构体还有2种 | |
| D. | 等物质的量的L、A和M 与足量浓溴水发生反应,消耗Br2的量之比为1:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
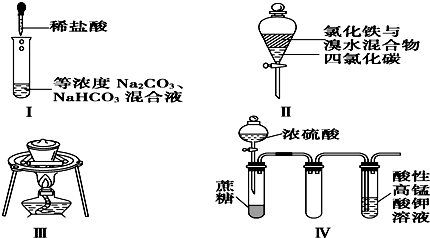
| A. | ②③ | B. | ①② | C. | ③④ | D. | ①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com