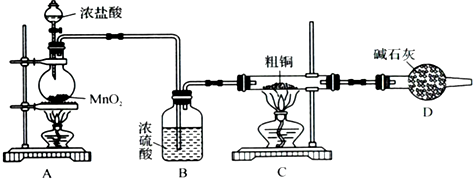
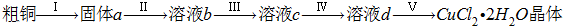氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品.某研究小组用粗铜(含杂质Fe)按如图1所示流程制备氯化铜晶体(CuCl
2?2H
20).
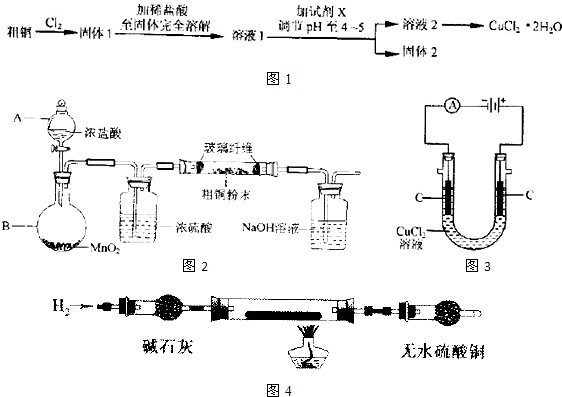
(1)实验室采用如图2所示的装置,可将粗铜与Cl
2反应转化为固体1(部分仪器和夹持装置已略去).
①装置B中发生反应的离子方程式是
MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
MnO
2+4H
++2Cl
-Mn
2++Cl
2↑+2H
2O
.
②有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装胃,你认为是否必要
否
否
(填“是”或“否”).
(2)试剂X用以除去杂质,X可选用下列试剂中的
cd
cd
(填序号).
a. NaOH b.NH
3?H
2O c.CuO d.Cu
2(OH)
2CO
3 e.CuSO
4(3)在溶液2转化为CuCl
2?2H
2O的操作过程中,发现溶液颜色出蓝色变为绿色.小组同学欲探究其原因.
己知:在氯化铜溶液中有如下转化关系:
Cu(H
2O)
42+(aq)(蓝色)+4Cl
-(aq)?CuCl
42-(aq)(黄色)+4H
2O(l)
①上述反应的化学平衡常数表达式是K=
| c(CuCl 42- ) |
| c[Cu(H2O) 42- ]?c4(Cl-) |
| c(CuCl 42- ) |
| c[Cu(H2O) 42- ]?c4(Cl-) |
.若增大氯离子浓度,K值(填“增大”、“减小”或“不变”)
不变
不变
.
②取氯化铜晶体配制成蓝绿色溶液Y,进行如下实验,其中能证明CuCl
2溶液中有上述转化关系的是(填序号)
abc
abc
.
a.将Y稀释,发现溶液呈蓝色
b.在Y中加入NaCl固体,溶液变为绿色
c.取Y进行电解,溶液颜色最终消失
(4)如图3所示,用石墨电极电解CuCl
2溶液,小组同学发现阴极碳棒上有红色和白色两种颜色的固体析出.有关文献资料表明,在铜和铜的化合物中Cu为紫红色,Cu
2O为红色,CuCl为白色,它们都不溶于水.
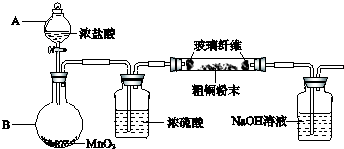
①小组同学将阴极碳棒洗涤干净并干燥后,放入玻璃管中,按如图4所示连接装置.排净装置中的空气后,充分加热,并将一张湿润的蓝色石蕊试纸置于装置末端的导管口附近.实验中发现,碳棒上的白色物质消失,红色物质依然存在;无色硫酸铜不变色,蓝色石蕊试纸变为红色.根据上述现象,玻璃管中发生反应的化学方程式为
.
②电解CuCl
2溶液时,阴极发生反应的电极方程式为
Cu2++2e-=Cu;Cu2++Cl-+e-=CuCl
Cu2++2e-=Cu;Cu2++Cl-+e-=CuCl
.


 CuCl42-(aq)+4H2O(l)的平衡常数为k=
CuCl42-(aq)+4H2O(l)的平衡常数为k=

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案


 CuCl42-(aq)+4H2O(l)
CuCl42-(aq)+4H2O(l)