
| A. | 从溴水中提取单质溴时,不能用无水乙醇代替CCl4 | |
| B. | 可用新制的Cu(OH)2悬浊液检验牙膏中存在的甘油 | |
| C. | 用纸层析法分离Cu2+和Fe3+,滤纸上端呈棕黄色,说明Fe3+在固定相中分配的更多 | |
| D. | 纸层析实验中,不能将滤纸上的试样点浸入展开剂中 |
分析 A.萃取剂不能和原溶剂互溶;
B.甘油与Cu(OH)2生成绛蓝色溶液;
C.滤纸上端呈棕黄色,说明Fe3+在流动相中分配的更多;
D.纸上层析法依据极性相似相溶原理,是以滤纸纤维的结合水为固定相,而以有机溶剂作为流动相,由于样品中各物质分配系数不同,因而扩散速度不同,从而达到分离的目的.
解答 解:A.乙醇和水互溶,所以不能作萃取剂,则乙醇不能代替四氯化碳,但可以用苯代替,故A正确;
B.甘油与Cu(OH)2生成绛蓝色溶液,所以可用新制的Cu(OH)2悬浊液检验牙膏中存在的甘油,故B正确;
C.用纸层析法分离Cu2+和Fe3+,滤纸上端呈棕黄色,说明Fe3+在流动相中分配的更多,随流动相移动的速度快一些,故C错误;
D.纸上层析中要求流动相溶剂对分离物质应有适当的溶解度,由于样品中各物质分配系数不同,因而扩散速度不同,所以纸上层析法是利用试样中各种离子随展开剂在滤纸上展开的速率不同而形成不同位置的色斑,如果试样接触展开剂,样点里要分离的离子或者色素就会进入展开剂,导致实验失败,故D正确;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及纸层析法、甘油的性质、萃取剂的选取等知识点,明确实验原理及物质性质是解本题关键,人教版教材不涉及纸层析法,对于部分学生来说较陌生,注意甘油和氢氧化铜反应现象,为易错点.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CS2为V形的极性分子 | B. | ClO3-的空间构型为三角锥形 | ||
| C. | SF6中有6对完全相同的成键电子对 | D. | PCl5和SO3均为非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
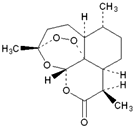 2015年我国女科学家屠呦呦因发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获诺贝尔奖.青蒿素结构式如图所示,下列关于青蒿素的说法不正确的是( )
2015年我国女科学家屠呦呦因发现青蒿素-一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获诺贝尔奖.青蒿素结构式如图所示,下列关于青蒿素的说法不正确的是( )| A. | 难溶于水,易溶于乙醚 | B. | 在热的NaOH溶液中可发生水解反应 | ||
| C. | 一定条件下能与氯气发生取代反应 | D. | 化学式为C15H21O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 负极发生的反应为Fe-2e-=Fe3+ | |
| B. | 正极发生的反应为2H2O+O2+4e-=4OH- | |
| C. | Cl-向负极迁移 | |
| D. | 铁锈是Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.0l mol•L-1•s-1 | B. | 0.002 mol•L-1•s-1 | ||
| C. | 0.06mol•L-•1s-1 | D. | 0.0025mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com