
【题目】某Na2SO3样品,其中可能含Na2SO4、K2SO4、K2CO3、NaCl中的一种或几种。为测定样品成分及其含量,称取样品5.0g,加入5mL 6mol/L的硫酸(过量),向逸出气体后的溶液中滴加足量BaCl2溶液,过滤得沉淀9.32g。取滤液作焰色反应实验,隔着蓝色钴玻璃观察无紫色。
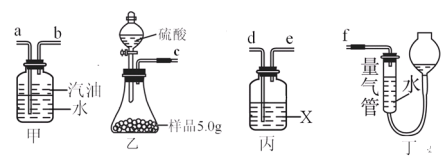
⑴用上图仪器组装实验,气流从左向右各管口连接顺序是 。
⑵甲中汽油的作用是 。丙中X液体是 。
⑶要准确测定生成气体的体积,乙中反应结束后,应进行的操作是 ,读数是应注意 。
⑷实验结束时测得丁中液体的体积为560mL(已换算成标准状况),根据实验现象推断该样品中一定不含 ,Na2SO3的质量分数为 ,Na2SO4的质量分数为 。
【答案】⑴c→d→e→b→a→f(2分)
⑵隔离气体和水,防止因气体被水吸收而造成实验误差(2分)浓硫酸(1分)
⑶上下移动量筒,使丁液面与甲中液面相平(1分)平视读出液体体积。( 1分)
⑷K2SO4和K2CO3(1分)Na2SO3:63.0%(2分)Na2SO4:28.4% (1分)
【解析】
试题分析:(1)该实验的流程为:气体发生-气体干燥-排液体测体积,根据发生装置、干燥装置、排水装置和收集装置排序,装置连接顺序接口为c→d→e→b→a→f;
(2)甲图中是排水量气测定二氧化硫的体积的装置,所以汽油是防止二氧化硫和水接触反应;X溶液是浓硫酸;
(3)排水量气装置测量气体的条件,利用的原理是气体排出液体进入量筒中读出液体的体积即为气体的体积;满足的条件是,冷却到室温,量筒和广口瓶液面相平,读出体积;
(4)加入6.0molL-1的硫酸至过量,若实验中加入硫酸溶液的体积为5.00mL,产生无色气体560mL(标准状况)二氧化硫物质的量为0.025mol;则亚硫酸钠的物质的量为0.025mol,质量分数=0.025mol×126g/mol/5.0g×100%=63%,得到白色沉淀9.32g,判断为硫酸钡沉淀物质的量=9.32g/233g/mol=0.04mol;加入的硫酸物质的量为0.03mol,说明一定含有硫酸钠,质量为0.01mol×142g/mol=1.42g,质量分数为1.42g/5g×100%=28.4%;亚硫酸钠的物质的量为0.025mol,质量=0.025mol×126g/mol=3.15g,固体质量为5.0g-1.42g-3.15g=0.43g,由焰色反应知无K2CO3、K2SO4,所以一定含有NaCl。


 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中的一定量混合气体发生反应:x A(g) + y B(g) ![]() z C(g),平衡时测得A的浓度为0.5 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再次达到平衡时,测得A的浓度降低为0.3 mol/L,下列有关判断正确的是( )
z C(g),平衡时测得A的浓度为0.5 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再次达到平衡时,测得A的浓度降低为0.3 mol/L,下列有关判断正确的是( )
A.x + y < z B.B的转化率降低
C.平衡向正反应方向移动 D.C的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是4种短周期元素,在元素周期表中的位置如下图所示,其中Z位于ⅦA族。下列判断错误的是( )
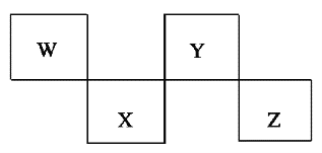
A. 常压下四种元素的单质中,W单质的熔点最高 B. Z的阴离子电子层结构与氩原子的相同
C. W的氢化物的沸点比Y的氢化物的沸点高 D. Y元素的非金属性比X元素的非金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生如下反应:mA(g)+nB(g)![]() pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是
A.m+n>p
B.平衡向逆反应方向移动
C.A的转化率降低
D.C的体积分数减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com