
分析 (1)气体分为单原子、双原子和多原子,含有分子的物质的量为1mol,而含有原子的物质的量不一定为1mol;
(2)常温常压下,气体摩尔体积不能使用22.4L/mol计算;
(3)标准状况下任何气体的气体摩尔体积都约为22.4L/mol;
(4)0.1molNaCl固体溶于1L水,所得溶液的体积不是1L;
(5)物质的量相的气体分子中含有的原子的物质的量不一定相同;
(6)苯的密度较小,需要从而从分液漏斗的上端倒出有机层.
解答 解:(1)在标准状况下,22.4L任何气体的物质的量为:$\frac{22.4L}{22.4L/mol}$=1mol,1mol气体含有原子的物质的量不一定为1mol,则含有原子数不一定为6.02×1023,故该说法错误,
故答案为:×;
(2)不是标准状况下,不能使用标准状况下的气体摩尔体积计算11.2L N2的物质的量,则含有的分子数不一定为0.5×6.02×1023,故该说法错误,
故答案为:×;
(3)标准状况下,1mol任何气体所占有的体积都约为22.4L,则标准状况时任何气体摩尔体积约为22.4L/mol,故该说法正确,
故答案为:√;
(4)0.1molNaCl固体溶于1L水,所得溶液的体积不是1L,所配制成的溶液浓度不是0.1mol/L,故该说法错误,
故答案为:×;
(5)气体分为单原子、双原子和多原子,则相同物质的量不同气体具有相同的原子数不一定相同,故该说法错误,
故答案为:×;
(6)用苯萃取碘水中的碘,溶有碘单质的有机层在上层,分液时有机层从分液漏斗的上端倒出,故该说法正确,
故答案为:√.
点评 本题考查了物质的量的计算及分液操作方法,题目难度不大,明确气体摩尔体积的使用条件为解答关键,注意掌握常见化学实验基本操作方法,试题培养了学生的灵活应用能力.


 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:解答题
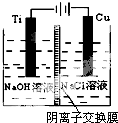 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:| 方法a | 用炭粉在高温条件下还原CuO |
| 方法b | 用葡萄糖还原新制的Cu(OH)2制备Cu2O; |
| 方法c | 电解法,反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑. |
| 方法d | 用肼(N2H4)还原新制的Cu(OH)2 |
| 序号 | 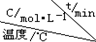 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
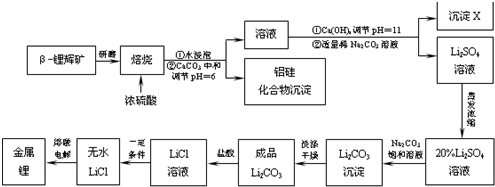
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 编号 | NaOH溶液的浓度(mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测HCl溶液的体积(mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
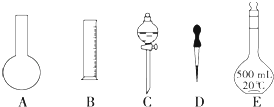
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某科研小组欲研究在其他条件不变的情况下,改变起始氧气的物质的量对合成新型硝化剂反应 4NO2(g)+O2(g)?2N2O5(g)△H<0的影响.
某科研小组欲研究在其他条件不变的情况下,改变起始氧气的物质的量对合成新型硝化剂反应 4NO2(g)+O2(g)?2N2O5(g)△H<0的影响.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

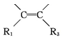 $→_{(2)Zn/H_{2}O}^{(1)O_{2}}$R1CHO+
$→_{(2)Zn/H_{2}O}^{(1)O_{2}}$R1CHO+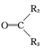
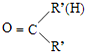 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$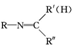 +H2O
+H2O  +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O
+H2O .
.  (写出其中一种的结构简式).
(写出其中一种的结构简式).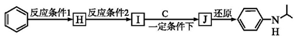 ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 臭氧具有氧化性,可用作自来水的消毒剂 | |
| B. | 活性炭具有还原性,可用作制糖业脱色剂 | |
| C. | 氢氟酸具有弱酸性,可用作玻璃的蚀刻剂 | |
| D. | 氨气具有弱碱性,可用作食品工业制冷剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuO、Na2O和Na2O2都是碱性氧化物 | |
| B. | SO2能与碱反应生成盐和水,因此SO2属于酸性氧化物 | |
| C. | NH4Cl不含金属阳离子,不属于盐 | |
| D. | 金属氧化物都是碱性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com