
| A. | 所用的氢氧化钠固体放置于空气中过久 | |
| B. | 定容时,眼睛俯视刻度线 | |
| C. | 洗涤烧杯和玻璃棒的溶液未转入容量瓶中 | |
| D. | 定容后摇匀,发现液面低于刻度线,不作处理 |
分析 根据c=$\frac{n}{V}$判断,造成浓度偏高,则可导致n偏大或V偏小,以此解答该题.
解答 解:A.氢氧化钠易变质,所用的氢氧化钠固体放置于空气中过久,则一定质量的样品中含有的氢氧化钠偏小,所配浓度偏低,故A不选;
B.定容时,眼睛俯视刻度线,导致体积偏小,则浓度偏大,故B选;
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中,则溶质的物质的量偏小,浓度偏低,故C不选;
D.定容后摇匀,发现液面低于刻度线,为正常操作,不作处理,溶液浓度不变,故D不选.
故选B.
点评 本题考查一定物质的量浓度溶液的配制过程中的误差分析,为高频考点,侧重考查学生的分析能力和实验能力,难度不大,注意实验的基本操作方法和注意事项.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | Na+、Al3+、Cl-、OH- | B. | H+、Na+、CO32-、NO3- | ||
| C. | Cu2+、K+、SO42-、NO3- | D. | Na+、H+、OH-、Ca2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知:正丁烷稳定性小于异丁烷,则CH3CH2CH2CH3(g)→(CH3)2CHCH3(g)△H>0 | |
| B. | 已知:OH-(ag)+H+(aq)═H2O(l)△H=-57.4 kJ/mol则含20.0g NaOH的稀溶液与稀醋酸完全中和,放出28.7kJ的热量 | |
| C. | 已知:2H2O(l)═2H2(g)+O2(g)△H=+483.6 kJ•mol-1,则氢气的燃烧热为241.8kJ/mol | |
| D. | 己知:2C(s)+2O2(g)═2CO2(g)△H1 2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | $\frac{c({H}^{+})•c(O{H}^{-})•c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$ | B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$ | ||
| C. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c({H}^{+})•c(O{H}^{-})}$ | D. | $\frac{c({H}^{+})•c(N{H}_{3}•{H}_{2}O)}{c(N{H}_{4}^{+})}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
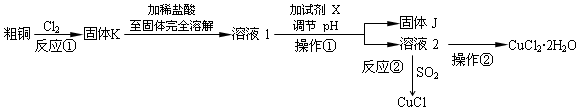
| 平行次数 | 1 | 2 | 3 |
| 0.250g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
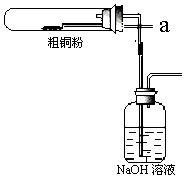
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 取20ml 0.1mol/L氨水溶液(其电离常数为K),用0.10mo/L盐酸滴定.滴定过程中溶液PH变化如图所示.图中a、b、c、d四个点所代表的溶液中,c(OH-)≈K的点是( )
取20ml 0.1mol/L氨水溶液(其电离常数为K),用0.10mo/L盐酸滴定.滴定过程中溶液PH变化如图所示.图中a、b、c、d四个点所代表的溶液中,c(OH-)≈K的点是( )| A. | a点 | B. | b点 | C. | c点 | D. | d点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Q1=Q3=197 kJ | B. | Q1=Q3<197 kJ | C. | 2Q2=Q1<197 kJ | D. | 2Q2<Q1<197 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | ①表示反应CO(g)+H2O(g)?CO2(g)+H2(g)中的△H大于0 | |
| B. | ②表示其它条件不变时,反应 4A(g)+3B(g)?2C(g)+6D(?)在不同压强下B% 随时间的变化,则D一定是气体 | |
| C. | ③表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 | |
| D. | ④表示10 mL 0.1mol/L Na2CO3和NaHCO3两种溶液中,分别滴加0.1mol/L HCl,产生CO2的体积随盐酸体积的变化,则b表示NaHCO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com