
【题目】新型冠状病毒肆虐全球,各国都在积极进行防疫工作,防疫环节中少不了对环境的消毒工作。下列物质不能用来进行消毒的是( )
A.臭氧B.75%的酒精C.氮气D.双氧水
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】海洋约占地球表面积的71%,具有巨大的开发潜力。
Ⅰ。海水淡化的方法主要有蒸馏法、电渗析法和离子交换法等。图为海水蒸馏原理示意图,请回答下列问题:

(1)冷却水的进水口是_______(填“a”或“b”);
(2)碎瓷片的作用是__________(填“防止暴沸”或“作催化剂”)。
Ⅱ。目前,从海水提取的溴占世界溴年产量的三分之一左右,空气吹出法是工业规模海水提溴的常用方法。其中一种工艺流程为:
①海水浓缩,酸化,
②通入Cl2,使Br—转化为Br2
③通入空气、水蒸气,将Br2吹入吸收塔,与吸收剂SO2反应转化为HBr;
④通入Cl2,再经过一系列处理得到产品Br2.
请回答下列问题:
(1)步骤②、③操作的目的是_____________(填“富集溴”或“萃取溴”);
(2)在步骤③中,生成HBr的化学方程式是________________;
(3)在步骤②中,若通入22.4L Cl2(标准状况),理论上可得到Br2___________g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①写出2-甲基丁烷的结构简式:_____ ②写出小苏打的化学式:_____
(2)写出铜与氯化铁溶液反应的离子方程式:_______________________________
(3)铁片、铜片链接后浸入稀硫酸形成原电池,正极反应式是______________
(4)写出苯和液溴在催化剂作用下生成溴苯的化学方程式____________________
(5)已知0.25mol N2H4(g)完全燃烧生成氮气和气态水时放出133.5KJ热量。写出该反应的燃烧热化学方程式____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)![]() 2Z(g),各组分在不同时刻的浓度如表,下列说法正确的是( )
2Z(g),各组分在不同时刻的浓度如表,下列说法正确的是( )
物质 | X | Y | Z |
初始浓度/mol/L | 0.1 | 0.2 | 0 |
2min末浓度/mol/L | 0.08 | a | b |
平衡浓度/mol/L | 0.05 | 0.05 | 0.1 |
A. 平衡时,X的转化率为20% B. t℃时,该反应的平衡常数为40
C. 增大平衡后的体系压强,v正增大,v逆减小,平衡向正反应方向移动 D. 前2min内,用Y的变化最表示的平均反应速率v(Y)=0.03mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素类化合物M具有抗病毒、抗癌等多种生物活性。下图是M和聚合物E的合成路线。
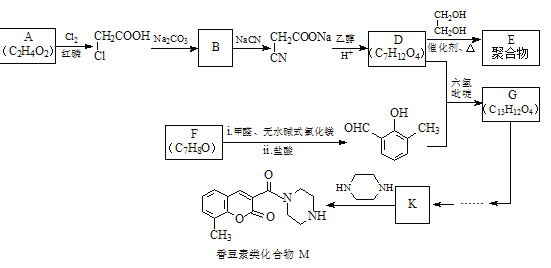
已知:
① ![]()
② ![]()
③ 
(1)A中官能团是_______。
(2)B→![]() 的反应类型是________。
的反应类型是________。
(3)化合物F能与FeCl3溶液发生显色反应,其结构简式是________。F有多种同分异构体,其中属于芳香族化合物、且为醇类物质的结构简式是________。
(4)G的结构简式是________。
(5)D→聚合物E的化学方程式是________。
(6)已知![]() ,将下列G→K的流程图补充完整:_____________________
,将下列G→K的流程图补充完整:_____________________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究不同条件下甘油(丙三醇)和辛酸酯化合成甘油二酯的最佳条件,科研工作者做了甘油二酯的酶法合成工艺研究。
实验1:研究不同投料比对产率的影响
(1)理论分析合成甘油二酯所需辛酸与甘油的投料比(物质的量之比)为2∶1。实验证明提高投料比,甘油二酯的产率会降低,其原因可能是_______。
实验2:研究吸水剂对反应的影响
(2)硅胶易与羟基结合,故有较强的亲水性,易于吸附水分子。但是在反应体系里加入硅胶后甘油二酯含量明显降低,说明合成甘油二酯的平衡发生了逆向移动,分析可能的原因是________。
实验3:研究不同催化剂的催化效果
曲线 | 催化剂 | 纵坐标 |
① | 脂肪酶I号 | 辛酸转化率 |
② | 脂肪酶II号 | 辛酸转化率 |
③ | 脂肪酶I号 | 甘油二酯含量 |
④ | 脂肪酶II号 | 甘油二酯含量 |

(3)其他条件相同时,不同脂肪酶(I号、II号)催化合成甘油二酯的效果如图所示,选择此实验中催化效果相对最佳的反应条件是________(填字母序号)。
A.12 h,I号 B.24 h,I号
C.12 h,II号 D.24 h,II号
实验4:研究温度对反应速率和产率的影响


(4)选定脂肪酶做催化剂,继续实验。
①综合上图,选择6 h时比较适宜的反应温度是________。
②在6 h之后,辛酸的转化率总趋势缓慢上升,30℃、40℃甘油二酯的含量上升,但是50℃的却有所降低,分析可能的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于元素周期表的说法正确的是( )
A.周期表的每一个纵列代表一个独立的族
B.主族元素中没有都是金属元素的族
C.副族元素都是金属元素
D.周期表共有14个族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经多年勘测,2018年11月23日省自然资源厅发布消息称在皖江地区发现特大铜矿床,具有重大实际意义。以黄铜矿(主要成分为CuFeS2,含有少量PbS、Al2O3、SiO2)为原料制取胆矾的流程如下图:

已知:常温下Ksp[Fe(OH)3]=8.0×10-38, Ksp[Al(OH)3]=3.0×10-33,Ksp[Cu(OH)2]=3.0×10-20。
(1)CuFeS2中硫元素的化合价为______,硫元素在周期表中的位置是______________。写出上述流程中生成亚硫酸铵的离子方程式:_______________________________。
(2)最适合的试剂A是________(写化学式)溶液,固体2的成份为PbSO4和_______。当试剂A的浓度为6mol·L-1时 ,“浸出”实验中,铜的浸出率结果如图所示。所采用的最佳实验条件(温度、时间)为_______________。

(3)最适合的试剂B是_______(填序号),最适合的试剂C是______(填序号),固体3的成份为_________________________。
a.Cl2 b.CuO c.酸性高锰酸钾溶液 d.NaOH e.H2O2 溶液 f.K2CO3
(4)操作1如在实验室中进行,用到的玻璃仪器有烧杯、玻璃棒和_______,操作2的步骤为________________过滤、洗涤。
(5)根据已知信息,请计算:当Fe3+完全沉淀时,溶液中Al3+理论最大浓度为______。(提示:当离子浓度≤1×10-5mol·L时,认为该离子沉淀完全)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种药物在临床上有许多的应用,具有去热、镇痛等疗效,以下是该药物的合成路线。

(1)化合物C的分子式为___________,B中含氧官能团的名称___________。
(2)F→G的反应类型为______________________。
(3)写出D→F的化学方程式____________________________________________。
(4)F的同分异构体有多种,符合以下条件的同分异构体有___________种,写出其中一种同分异构体的结构简式______________________。
①属于芳香族化合物,苯环上只有两个支链,苯环上的一氯代物只有两种。
②能与FeCl3溶液发生显色反应。
③能与碳酸氢钠反应产生气体。
(5)写出由2—溴丁烷、丙烯酸和乙醇为原料合成![]() 的合成路线(其他试剂任选)。
的合成路线(其他试剂任选)。
_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com