
【题目】设pC为溶液中粒子物质的量浓度的负对数,即:pC=- lg C。25℃时,某浓度的H2R水溶液中,pC(H2R),pC(HR-)、pC(R2-)随溶液pH的变化曲线如图所示。下列说法正确的是
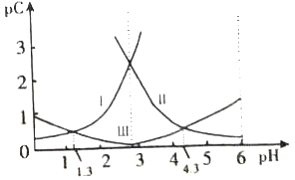
A. 曲线Ⅰ表明,c(R2-)随着pH增大而逐渐增大
B. pH=1.3时,3 c(R2-)+c(OH-)=10-1.3mol`L-1
C. NaHR水溶液中:c(Na+)>c(HR-)>c(OH-)>c(H+)
D. 常温下,该体系中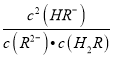 =1000
=1000
【答案】D
【解析】H2RH++HR-,HR-H++R2-,pH增加促进电离平衡正向移动,所以由图可知:曲线Ⅰ是H2R的物质的量浓度的负对数,曲线Ⅱ是R2-的物质的量浓度的负对数,曲线Ⅲ是HR-的物质的量浓度的负对数。A. 曲线Ⅰ是H2R的物质的量浓度的负对数,故A错误;B. pH=1.3时,c(HR-)=c(H2R),根据电荷守恒,c(HR-)+2 c(R2-)+ c(OH-) =c(H+),即c(H2R) +2 c(R2-)+ c(OH-) =10-1.3mol`L-1,而此时c(H2R)<c(R2-),因此3 c(R2-)+c(OH-)<10-1.3mol`L-1,故B错误;C.根据图像,pH=1.3时,c(HR-)=c(H2R),Ka1=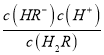 = c(H+)=10-1.3,pH=4.3时,c(HR-)=c(R2-),Ka2=
= c(H+)=10-1.3,pH=4.3时,c(HR-)=c(R2-),Ka2=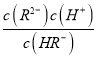 = c(H+)=10-4.3,则NaHR的水解平衡常数Kh=
= c(H+)=10-4.3,则NaHR的水解平衡常数Kh=![]() =10-12.7,因此NaHR的电离程度>水解程度,溶液显酸性,NaHR水溶液中 c(H+)>c(OH-),故C错误;D. 常温下,该体系中
=10-12.7,因此NaHR的电离程度>水解程度,溶液显酸性,NaHR水溶液中 c(H+)>c(OH-),故C错误;D. 常温下,该体系中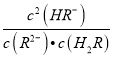 =
=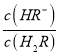 ×
×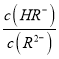 =
=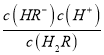 ×
× =
=![]() =
=![]() =1000,故D正确;故选D。
=1000,故D正确;故选D。


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
【题目】下列关于SO2性质的说法中,不正确的是
A. 能使品红溶液褪色 B. 能与水反应生成硫酸
C. 能与NaOH溶液反应 D. 能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A(C9H18O2)在稀硫酸溶液中水解为相对分子质量相等的B、C,其中B分子中含有 3个甲基,则A、B、C中能与氢氧化钠溶液反应的物质最多有(不考虑立体异构)
A. 10种 B. 8种 C. 6种 D. 4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是食用碘盐包装上的部分说明,下列说法正确的是( )
配料:精盐、碘酸钾、抗结剂
碘含量:35±15 mg/kg
储存方法:密封、避光、防潮
食用方法:烹饪时,待食品熟后加入碘盐
A.高温会导致碘的损失
B.碘酸钾可氧化氯化钠
C.可用淀粉检验碘盐中的碘酸钾
D.该碘盐中碘酸钾含量为20~50 mg/kg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列符合未来新能源特点的是( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A. ①②③④ B. ⑤⑥⑦⑧ C. ①③⑥⑧ D. ②④⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于水和无机盐的叙述中,错误的是
A. 无机盐是细胞中能源物质之一 B. 水在维持细胞形态中有重要作用
C. 某些无机盐参与构成细胞复杂化合物 D. 水在活细胞中主要以自由水形式存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组欲测定某已部分变质的小苏打样品中Na2CO3的质量分数,设计如下实验方案。
【方案一】称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为_______________。
(2)实验中,需加热至恒重的目的是_______________。
【方案二】称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-==BaCO3↓+H2O)
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为_______________。
(3)实验中判断沉淀是否完全的方法是_______________。
【方案三】按如下图所示装置进行实验:
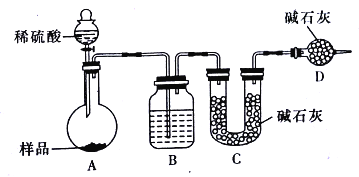
(1)D装置的作用是_______________。分液漏斗中_________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重8.80g,则样品中Na2CO3的质量分数为________________(保留三位有效数字)
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存的在一个明显缺陷是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知(HF)2(g)2HF(g),△H>0,且平衡体系的总质量[m(总)]与总物质的量[n(总)]之比在不同温度下随压强的变化曲线如图所示.下列说法正确的是( ) 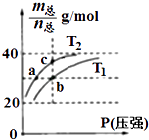
A.温度:T1<T2
B.平衡常数:K(a)=K(b)<K(c)
C.反应速率:Vb>Va
D.当 ![]() =30g/mol时,n(HF):n(HF)2=2:1
=30g/mol时,n(HF):n(HF)2=2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com