
| t/s | 2 | 4 | 7 | 9 |
| n£ØY£©/mol | 0.12 | 0.10 | 0.09 | 0.09 |
| A”¢·“Ó¦Ē°2sµÄĘ½¾łĖŁĀŹv£ØZ£©=2.0”Į10-3 mol/£ØL?s£© |
| B”¢ĘäĖūĢõ¼ž²»±ä£¬¼ÓČėŅ»¶ØĮæµÄY£¬·“Ó¦ĖŁĀŹŅ»¶Ø¼Óæģ |
| C”¢·“Ó¦½ųŠŠ4sŹ±£¬XµÄ×Ŗ»ÆĀŹ75% |
| D”¢·“Ó¦“ļµ½Ę½ŗāŹ±£¬XµÄĪļÖŹµÄĮæÅضČĪŖ0.02mol?L-1 |
| ||
| ”÷t |
| ×Ŗ»ÆµÄĪļÖŹµÄĮæ |
| ĘšŹ¼ĪļÖŹµÄĮæ |
| n |
| V |
| ||
| ”÷t |
| ||
| 2s |
| ×Ŗ»ÆµÄĪļÖŹµÄĮæ |
| ĘšŹ¼ĪļÖŹµÄĮæ |
| 0.12mol |
| 0.16mol |
| n |
| V |
| 0.02mol |
| 10L |


 ĘŚÄ©ŗĆ³É¼ØĻµĮŠ“š°ø
ĘŚÄ©ŗĆ³É¼ØĻµĮŠ“š°ø 99¼Ó1ĮģĻČĘŚÄ©ĢŲѵ¾ķĻµĮŠ“š°ø
99¼Ó1ĮģĻČĘŚÄ©ĢŲѵ¾ķĻµĮŠ“š°ø °ŁĒæĆūŠ£ĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
°ŁĒæĆūŠ£ĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø ŗĆ³É¼Ø1¼Ó1ĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
ŗĆ³É¼Ø1¼Ó1ĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø ½š×“ŌŖ¼ØÓÅŗĆ¾ķĻµĮŠ“š°ø
½š×“ŌŖ¼ØÓÅŗĆ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
A”¢MnO2+4HCI£ØÅØ£©
| ||||
BӢSiO2+NaCO3
| ||||
| C”¢2KCIO3+I2=2KIO3+CI2”ü·Ē½šŹōŠŌ£ŗI£¾Cl | ||||
DӢCO2+2Mg
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢µē½ā·Ø¾«Į¶Ķ£¬µ±Ńō¼«ÖŹĮæ¼õÉŁ 64g Ź±£¬ĶāµēĀ·Ķعżµē×ÓŹżĪŖ 2NA |
| B”¢25”ꏱ£¬1LpH=3 µÄ“×ĖįČÜŅŗÖŠŗ¬ÓŠ“×Ėį·Ö×ÓŹż“óÓŚ 0.001NA |
| C”¢1L0.1 mol?L-1NaClO ČÜŅŗÖŠŗ¬ ClO-ŹżÄæĪŖ 0.1NA |
| D”¢ŅŃÖŖ N2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92.2kJ?mol-1£¬µ±·“Ó¦·ÅČČ73.76kJŹ±£¬¹²ŠĪ³É H-H ¼ü 2.4NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
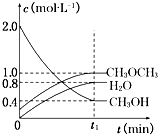
 °ŃĆ¾ĢõĶ¶Čėµ½Ź¢ÓŠŃĪĖįµÄ³ØæŚČŻĘ÷Ąļ£¬²śÉśH2µÄĖŁĀŹČēĶ¼ĖłŹ¾£¬ŌŚĻĀĮŠŅņĖŲÖŠ£¬Ó°ĻģO”«t1Ź±¼ä¶Ī·“Ó¦ĖŁĀŹµÄÖ÷ŅŖŅņĖŲŹĒ£Ø””””£©
°ŃĆ¾ĢõĶ¶Čėµ½Ź¢ÓŠŃĪĖįµÄ³ØæŚČŻĘ÷Ąļ£¬²śÉśH2µÄĖŁĀŹČēĶ¼ĖłŹ¾£¬ŌŚĻĀĮŠŅņĖŲÖŠ£¬Ó°ĻģO”«t1Ź±¼ä¶Ī·“Ó¦ĖŁĀŹµÄÖ÷ŅŖŅņĖŲŹĒ£Ø””””£©| A”¢ŃĪĖįµÄÅØ¶Č |
| B”¢Ć¾ĢõµÄ±ķĆ껿 |
| C”¢Cl-µÄÅØ¶Č |
| D”¢ČÜŅŗµÄĪĀ¶Č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
A”¢N2µÄµē×ÓŹ½£ŗ | ||
| B”¢106gµÄŅŅ“¼ŗĶ±ū“¼»ģŗĻŅŗĶźČ«Č¼ÉÕÉś³ÉµÄCO2ĪŖ112L£Ø±ź×¼×“æö£© | ||
C”¢ĮŚōĒ»ł±½¼×ĖįµÄ½į¹¹¼ņŹ½£ŗ | ||
D”¢ÖŹ×ÓŹżĪŖ53£¬ÖŠ×ÓŹżĪŖ78µÄµāŌ×Ó£ŗ
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| 1 |
| 2 |
| 1 |
| 2 |
| A”¢¢Ł | B”¢¢Ś¢Ü | C”¢¢Ū¢Ü | D”¢¢Ł¢Ś¢Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| c(CO2)?c(NO) |
| c(NO2)?c(CO) |
| A”¢øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗNO2+COØTCO2+NO |
| B”¢øĆ·“Ó¦µÄģŹ±äĪŖøŗÖµ |
| C”¢ÉżøßĪĀ¶Č£¬Õż·“Ó¦ĖŁĀŹ¼õŠ” |
| D”¢ŗćĪĀŹ±£¬Ōö“óŃ¹Ē棬ŃÕÉ«¼ÓÉī£¬ŅņĘ½ŗā×óŅĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢0.1 mol/£ØL?S£© |
| B”¢0.05mol/£Ø L?min£© |
| C”¢0.05mol/£ØL?s£© |
| D”¢0.8mol/£ØL?S£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 £Ø1£©Ņ»¶ØĢõ¼žĻĀ£¬NOÓėNO2“ęŌŚĻĀĮŠ·“Ó¦£ŗNO£Øg£©+NO2£Øg£©?N2O3£Øg£©£¬ĘäĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK=
£Ø1£©Ņ»¶ØĢõ¼žĻĀ£¬NOÓėNO2“ęŌŚĻĀĮŠ·“Ó¦£ŗNO£Øg£©+NO2£Øg£©?N2O3£Øg£©£¬ĘäĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK=²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com