
| A. | 1.6mol | B. | 大于1.2 mol | C. | 大于1.6 mol | D. | 小于1.2 mol |
分析 依据化学反应速率的概念进行分析计算,并注意浓度越大,反应速率越大来解答.
解答 解:进行到4min时,测得n (SO2)=0.4mol,此时反应的速率为V(SO2)=$\frac{\frac{2mol-0.4mol}{2L}}{4min}$=0.2mol/L•min;反应进行到前2min末时设二氧化硫物质的量为x,依据速率定义可得V′(SO2)=$\frac{\frac{2mol-xmol}{2L}}{2min}$;进行到2min时的物质浓度大于4min时的物质的浓度,所以反应时4min的反应速率小于2min的反应速率,即V′(SO2)=$\frac{\frac{2mol-xmol}{2L}}{2min}$>0.2mol/L•min;整理得,x<1.2mol,
故选D.
点评 本题考查了化学反应速率的概念应用,化学反应速率的影响因素,主要是浓度对速率的影响判断.


科目:高中化学 来源: 题型:选择题
| A. | 若两烧杯中铝粉均已完全溶解,则两烧杯中放出氢气的量相同 | |
| B. | 若两烧杯中铝粉均未完全溶解,则盛氢氧化钠溶液的烧杯中放出氢气的量更多 | |
| C. | 若反应后,有一个烧杯中铝粉完全溶解,另一个烧杯中铝粉没有完全溶解,则那个还有铝没有溶解的烧杯原来盛着的是氢氧化钠溶液 | |
| D. | 无论如何,盐酸与铝粉反应产生的H2不可能比氢氧化钠溶液与铝粉反应产生的H2多 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
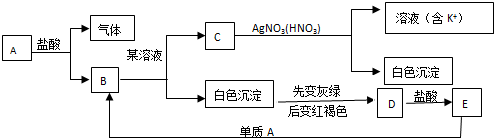
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH和HAC | B. | KOH和HNO3 | C. | Ba(OH)2和H2SO4 | D. | NH3•H2O和HAC |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com