
����Ŀ���Թ�����Ϊ�����������������V2O5���ǽӴ�����������Ĵ������ӷϷ������л���V2O5�ȱ�����Ⱦ��������������Դ�ۺ����á��Ϸ���������Ҫ�ɷ�Ϊ��
���� | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
��������/% | 2.2��2.9 | 2.8��3.1 | 22��28 | 60��65 | 1��2 | <1 |
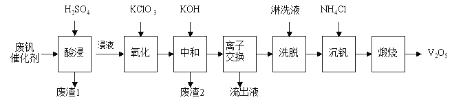
������һ�ַϷ��������չ���·�ߣ�
�ش��������⣺
��1���������ʱV2O5ת��ΪVO2+����Ӧ�����ӷ���ʽΪ___________��ͬʱV2O4ת��VO2+��������1������Ҫ�ɷ���__________________��
��2��������������ʹ3 mol��VO2+��ΪVO2+������Ҫ������KClO3����Ϊ____________mol��
��3�����к͡�����֮һ��ʹ����V4O124-��ʽ��������Һ�С�������2���к���_____________��
��4�������ӽ������͡�ϴ�ѡ��ɼ�ʾΪ��4ROH+![]()
![]() R4V4O12+4OH����ROHΪǿ���������ӽ�����֬����Ϊ�����ϴ��Ч�ʣ���ϴҺӦ�ó�___________�ԣ���ᡱ������С�����
R4V4O12+4OH����ROHΪǿ���������ӽ�����֬����Ϊ�����ϴ��Ч�ʣ���ϴҺӦ�ó�___________�ԣ���ᡱ������С�����
��5��������Һ����������������________��
��6�����������õ�ƫ����泥�NH4VO3��������д�������ա��з�����Ӧ�Ļ�ѧ����ʽ____________��
���𰸡���1��V2O5��2H��=2VO2����H2O��SiO2 ��2��0.5 ��3��Fe(OH)3��Al(OH)3
��4���� ��5��K�� ��6��2NH4VO3![]() V2O5��H2O����2NH3����
V2O5��H2O����2NH3����
��������
�����������1���������ʱV2O5ת��ΪVO2+��VԪ�ػ��ϼ۲��䣬˵������������ԭ��Ӧ������ԭ���غ��֪��Ӧ�����ӷ���ʽΪV2O5��2H��=2VO2����H2O���������������Ӧ������1������Ҫ�ɷ��Ƕ������衣
��2��������������ʹ3 mol��VO2+��ΪVO2+��VԪ�ػ��ϼ۴ӣ�4�����ߵ���5�ۣ���������KClO3����Ԫ�ػ��ϼ۴ӣ�5�۽��͵���1�ۣ����ݵ��ӵ�ʧ�غ��֪��Ҫ����ص����ʵ���Ϊ��3mol��6��0.5mol��
��3�����к͡�����֮һ��ʹ����V4O124��ʽ��������Һ�У�ͬʱ��������������������������������2���к���Fe(OH)3��Al(OH)3��
��4�����ݷ���ʽ��֪Ϊ�����ϴ��Ч�ʣ���ӦӦ�����淴Ӧ������У������ϴҺӦ�óʼ��ԡ�
��5������ǰ�����������غ��������أ�������Һ���������������Ǽ����ӡ�
��6������ԭ���غ��֪ƫ����泥�NH4VO3�������ա�����������������������ˮ��������Ӧ�Ļ�ѧ����ʽΪ2NH4VO3![]() V2O5��H2O����2NH3����
V2O5��H2O����2NH3����


 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ǿ������Һ���ܴ�������������ǣ� ��
A��S2�� B��AlO2�� C��HCO3�� D��NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʵľ����У���ѧ�����ͺ;������Ͷ���ͬ����
A��CO2��H2S B��KOH��CH4 C��Si��CO2 D��NaCl��HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йطǽ������仯�����˵����ȷ���ǣ� ��
A. �����ʹ��ɫʯ����Һ���ɫ
B. ��������ͨ����ɫʯ����Һ�У���Һ�ȱ�����ɫ
C. ����п����ϡ���ᷴӦ�Ʊ�����
D. Һ���ӷ������Դ��Һ����Լ�ƿ��Ӧ��ˮ�Ᵽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵��û�п�ѧ�Դ������ �� ��
A. ����ѩ����Ư�ۿ���������ɫ������Ȼʧ��ɫ����û����ף�ֻ�и���
B. CO�ж�������ú¯�ľ��ң��ɷ���������ˮ����������Ч������CO����ֹú���ж�
C. �Ȼ��ƾ�����ˮ�Ժͳ����ԣ�������������ˮ��Һ��������·������Ч�ر���·��
D. ��Ԫ���ж�����ֹ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������۷��������ᡢMgCl2��Һ��FeCl3��Һ��CuCl2��Һ��ɵĻ��Һ�У���ַ�Ӧ��������ʣ�࣬����Һ�к��е��������ǣ� ��
A. Cu2+��Fe2+ B. H+��Cu2+ C. Fe3+��Fe2+ D. Fe2+��Mg2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������ܱ������У��������»�ѧ��Ӧ��CO2(g)+H2(g) ![]() CO(g)+H2O(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO(g)+H2O(g)���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
��ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK�� ��
��2���÷�ӦΪ ��Ӧ��������������������������
��3��830������1L�Ĺ̶��������ܱ������з���1 mol CO��5 mol H2O����Ӧ��ƽ����仯ѧƽ�ⳣ��K 1.0����������������С����������������
��4��830���������еķ�Ӧ�ﵽƽ�⡣�������������������£����������������ƽ�� �ƶ��������������������������淽��������������
��5����1200��ʱ����ijʱ�̸�������CO2��H2��CO��H2O��Ũ�ȷֱ�Ϊ2 mol��L��1��2 mol��L��1��4 mol��L��1��4 mol��L��1�����ʱ������Ӧ��ƽ���ƶ�����Ϊ ��ѡ��������Ӧ�����������淴Ӧ�������������ƶ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������з�����ѧ��ӦH2��g��+I2��g��2HI��g��,05min��H2��Ũ�ȼ�����0.1mol/L���������ʱ���ڣ���HI��ʾ��ƽ����Ӧ����Ϊ�� ��
A��0.01molL-1min-1 B��0.2molL-1min-1
C��0.04molL-1min-1 D��0.5molL-1min-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(C1NO)���л��ϳ��е���Ҫ�Լ�������NO��Cl2��ͨ�������·�Ӧ�õ�����ѧ����ʽΪ2NO(g)+C12(g)![]() 2C1NO(g)��
2C1NO(g)��
��1�����������������ڴ����еĺ������������ʱ�������������ȣ��漰���·�Ӧ��
�� 2NO2(g)+NaC1(s)![]() NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
�� 4NO2(g)+2NaC1(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2
�� 2NO(g)+C12(g)![]() 2C1NO(g) K3
2C1NO(g) K3
��K1��K2��K3֮��Ĺ�ϵΪK3=______________��
��2����֪���ֻ�ѧ���ļ����������±�(�������ȵĽṹΪCl-N=O):

��2NO(g)+C12(g)![]() 2C1NO(g)��Ӧ����H��a�Ĺ�ϵΪ��H=________kJ/mol��
2C1NO(g)��Ӧ����H��a�Ĺ�ϵΪ��H=________kJ/mol��
��3����1L�ĺ����ܱ������г���2molNO(g)��1molC12(g)���ڲ�ͬ�¶��²��c(C1NO)��ʱ��Ĺ�ϵ��ͼA:

�� ��ͼA���ж�T1 ________T2���÷�Ӧ����H________0 (����>����<������=��)��
�� ��Ӧ��ʼ��10minʱNO��ƽ����Ӧ����v(NO)=____________mol/(L��min)��
�� T2ʱ�÷�Ӧ��ƽ�ⳣ��K=____________��
��4�� һ���������ں��º��ݵ��ܱ������а�һ����������NO(g)��Cl2(g)��ƽ��ʱClNO�����������n(NO)/n(C12)�ı仯ͼ����ͼB����A��B��C��״̬�У�NO��ת����������________�㡣
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com