
| X | Y | ||
| Z | W |
| A�� | ԭ�Ӱ뾶��С�����˳��ΪX��Y��Z��W | |
| B�� | YԪ������������Ӧ��ˮ���ﻯѧʽΪH3YO4 | |
| C�� | X��Z����Ԫ�ص���������������ѧ��������ͬ | |
| D�� | Y�����̬�⻯���Y��������ͬ����Ԫ����̬�⻯������ȶ� |
���� X��Y��Z��WΪ���ֶ�����Ԫ�أ������������ڱ�λ�ÿ�֪��X��Y���ڵڶ����ڣ�Z��W���ڵ������ڣ���Ԫ��λ���������ĸ����壬ZԪ��ԭ���������������ڲ����������$\frac{1}{5}$������������Ϊ$\frac{2+8}{5}$=2����ZΪMg����WΪAl��XΪC��YΪN���ݴ˽��
��� �⣺X��Y��Z��WΪ���ֶ�����Ԫ�أ������������ڱ�λ�ÿ�֪��X��Y���ڵڶ����ڣ�Z��W���ڵ������ڣ���Ԫ��λ���������ĸ����壬ZԪ��ԭ���������������ڲ����������$\frac{1}{5}$������������Ϊ$\frac{2+8}{5}$=2����ZΪMg����WΪAl��XΪC��YΪn��
A��ͬ���ڴ�������ԭ�Ӱ뾶�ڼ�С��ͬ�������϶���ԭ�Ӱ뾶������ԭ�Ӱ뾶ΪY��X��W��Z����A����
B��YΪNԪ�أ�����������Ӧ��ˮ���ﻯѧʽΪHNO3����B����
C��X��������ΪCO��CO2��Z��������ΪNa2O��Na2O2��CO��CO2�к��й��ۼ��������ƺ��������к������Ӽ�����C����
D��ͬ�������϶��·ǽ����Լ������⻯���ȶ�����Ԫ�طǽ�����һ�£���Y�����̬�⻯���Y��������ͬ����Ԫ����̬�⻯������ȶ�����D��ȷ��
��ѡD��
���� ���⿼��λ�ýṹ���ʹ�ϵӦ�ã���ȷԪ�ص��ƶ��ǽ����Ĺؼ������ض�Ԫ�������ɵĿ��γ̣��ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
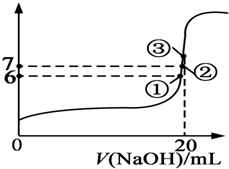 25��ʱ����20mL 0.1mol/L���������Һ�м���VmL 0.1mol/L NaOH��Һ����û����Һ��pH�仯����ͼ��ʾ������˵����ȷ���ǣ�������
25��ʱ����20mL 0.1mol/L���������Һ�м���VmL 0.1mol/L NaOH��Һ����û����Һ��pH�仯����ͼ��ʾ������˵����ȷ���ǣ�������| A�� | pH=3��HF��Һ��pH=11��NaF��Һ�У���ˮ�������c��H+����� | |
| B�� | �ڢٵ�ʱpH=6����Һ�У�c��F-��-c��Na+��=9.9��10-7mol/L | |
| C�� | �ڢڵ�ʱ����Һ�У�c��F-����c��Na+�� | |
| D�� | �ڢ۵�ʱV=20mL����Һ�У�c��F-����c��Na+��=0.1mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
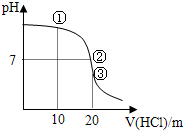
| A�� | ����Һ��c��Cl-����c��NH4+����c��OH-����c��H+�� | |
| B�� | ����Һ��c��NH4+��=c��Cl-��=c��OH-��=c��H��+ | |
| C�� | ����Һ�����е�����Ϊ5�� | |
| D�� | �ζ������п��ܳ��֣�c��NH4+����c��OH-����c��Cl-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʹ�õ�ʯ�͡�ú�ȴ�ͳ��Դ���������ܡ����ܵ�����Դ����������Щ��Դ������̫����ת���� | |
| B�� | ��������һ�����ܵ������ﱡĤ���м�ǿ�Ŀ���ʴ������������������������������ԡ�������ʳƷ�� | |
| C�� | �������ò�ľ�������ɻ�����ũҵ���ø������ֽ��֣���ҵ�����������δ���Ƥ��ȣ�����̵Ĺ�ͬ�㶼�������˵����ʱ��Ե����� | |
| D�� | �������������Ρ��������ȵȺ��Ȼ����ﶼ����ǿ�����ԣ�������ɱ���������Ȼ��ء������Ҳ�Ǻ��Ȼ������Ҳ������ɱ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ϊ21�ļ�ԭ�ӣ�${\;}_{19}^{40}$K | |
| B�� | �Ȼ����ĵ���ʽ��Ba2+[${\;}_{•}^{•}$$\underset{\stackrel{••}{ci}}{••}$${\;}_{•}^{•}$]${\;}_{2}^{-}$ | |
| C�� | N3-�Ľṹʾ��ͼ��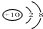 | |
| D�� | ��2-��-1��3-����ϩ�Ľṹ��ʽ��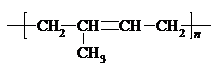 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
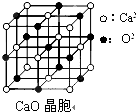 [���ʽṹ������]���������з�Ӧ�ϳ������谷��
[���ʽṹ������]���������з�Ӧ�ϳ������谷��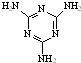 ���׳ơ����������������������谷���������ᣨ
���׳ơ����������������������谷���������ᣨ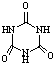 �������������������谷�����֮��ͨ�����Ӽ������ϣ������������γɽ�ʯ��
�������������������谷�����֮��ͨ�����Ӽ������ϣ������������γɽ�ʯ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ���������c��H+ ��=l.0xl0-12 mol/L | |
| B�� | c ��CH3COOH����c ��H+ ����c ��CH3COO- ����c ��OH-�� | |
| C�� | ��ͬŨ�ȵ�����ֱ��ˮϡ��10����pH �����ᣩ��pH �����ᣩ | |
| D�� | ������������������Һ��Ӧ��c ��CH3COOH��+c ��CH3COO- ��=0.01mol/L�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
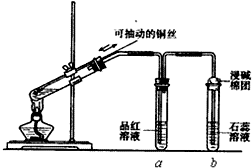 ijͬѧ���ʵ��֤��ͭ��Ũ�����ܷ�����Ӧ��������������������ʣ���ͼ��ʾ�����Թ������2mLŨ���ᣬ�ô����ܺ�һ��С�Ľ����������ӿ��в���һ��ͭ˿�����ȣ��ѷų�����������ͨ��Ʒ����Һ��ʯ����Һ�У�
ijͬѧ���ʵ��֤��ͭ��Ũ�����ܷ�����Ӧ��������������������ʣ���ͼ��ʾ�����Թ������2mLŨ���ᣬ�ô����ܺ�һ��С�Ľ����������ӿ��в���һ��ͭ˿�����ȣ��ѷų�����������ͨ��Ʒ����Һ��ʯ����Һ�У��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӹ���֮��Ϊ1��1 | B�� | ���ʵ���֮��Ϊ1��1 | ||
| C�� | ���֮��Ϊ11��16 | D�� | ������֮��Ϊ1��1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com