
����Ŀ��������I�Ǻϳɺ���Ԫ����������һ���м��塣����Robinson�ɻ���Ӧ�ϳ�I��·�����£��ش��������⣺

��֪����![]()
��
��1��B��C�ķ�Ӧ����ʽΪ________��
��2��������E��I�Ľṹ��ʽ�ֱ���________��________��
��3��C��D��F��G�ķ�Ӧ���ͷֱ���________��________��
��4��д����������������G��ͬ���칹��Ľṹ��ʽ________��
��������������ȫ��Ӧʱ���������ʵ���֮��Ϊ1:3������4�ֲ�ͬ��ѧ�������⡣
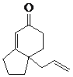
��5��д���Լ״��������ᡢ���������![]() Ϊԭ�Ϻϳ�
Ϊԭ�Ϻϳ� �ĺϳ�·�ߣ������Լ���ѡ����______________________________________��
�ĺϳ�·�ߣ������Լ���ѡ����______________________________________��
���𰸡�![]()
![]()
 ������Ӧ ȡ����Ӧ
������Ӧ ȡ����Ӧ 
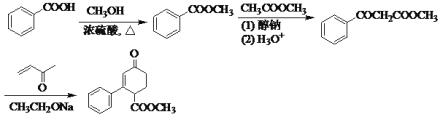
��������
����֪�����ٺ�E����ʽ��֪EΪ![]() ��D��״�����������Ӧ�õ�E����DΪHOOCCH2CH2CH2CH2COOH��C����������Һ������Ӧ�õ�D����CΪ
��D��״�����������Ӧ�õ�E����DΪHOOCCH2CH2CH2CH2COOH��C����������Һ������Ӧ�õ�D����CΪ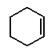 ����BΪ
����BΪ![]() ��AΪ�����飬����֪�����ڿ�֪H�뾭��Ӧ�ڵõ�I����I�ṹ��ʽΪ
��AΪ�����飬����֪�����ڿ�֪H�뾭��Ӧ�ڵõ�I����I�ṹ��ʽΪ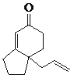 ���Դ˷�����
���Դ˷�����
��1��B���������ƴ���Һ��ȥ�õ�C ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��2��������������֪������E��I�Ľṹ��ʽ�ֱ���![]() ��
�� ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
�� ��
��
��3��C����������Һ������Ӧ�õ�D���ɷ�Ӧ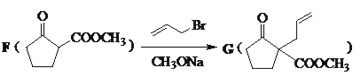 ��֪F��Hԭ�ӱ�
��֪F��Hԭ�ӱ�![]() ȡ�����ʴ�Ϊ��������Ӧ��ȡ����Ӧ��
ȡ�����ʴ�Ϊ��������Ӧ��ȡ����Ӧ��
��4��G��ͬ���칹����Ϣ�������������ȫ��Ӧʱ���������ʵ���֮��Ϊ1:3��G����ຬ��һ���������Ȼ�����ض����з��ǻ���G�к���4�������Ͷȣ���G��ͬ���칹��������ⲻ���в����ͼ�������4�ֲ�ͬ��ѧ������������������� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��5����������״�����������Ӧ�õ�![]() ������֪��Ӧ��
������֪��Ӧ��![]() �����������Ӧ�õ�
�����������Ӧ�õ�![]()
![]() ��
��![]() ��Ӧ�õ�
��Ӧ�õ�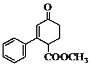 ���ϳ�·�߳�ͼΪ��
���ϳ�·�߳�ͼΪ��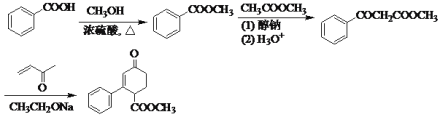 ���ʴ�Ϊ��
���ʴ�Ϊ��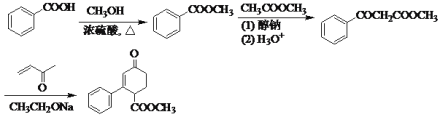 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������̼���ɼ��������ͼ��ʾ��NAΪ�����ӵ�������ֵ������˵����ȷ����
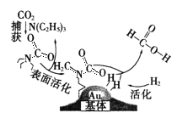
A.10.1gN(C2H5)3������һ���������γ��Σ�����[N(C2H5)3H]+����ĿΪ0.1NA
B.30g��������У����Ӷ���ĿΪ5 NA
C.�ڲ�������У�����22.4L CO2����״�������뷴Ӧ�����ڷ�Ӧ������CO2����ֻ����NA�Ե��Ӷ�
D.�÷�Ӧ��������ԭ��Ӧ��ÿ����1mol���ᣬת�Ƶĵ�����Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����
A.��״���£�1�������������Ϊ ![]() cm3
cm3
B.ͭ��⾫��ʱ����������������64 gʱ����·��ת�Ƶ�����Ϊ2NA
C.��״����22.4 L Cl2��ȫ����ˮʱ��������Һ�к���������Ϊ2NA
D.NaCl������Na+�����Cl���ĺ˼����Ϊa cm�����侧���ܶ�Ϊ ![]() g��cm��3
g��cm��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ���ѧ�ҳɹ��ϳ��˼������ӵ���ĸ��ѿ����ӻ�����(CH3NH3)PbI3������������нϸߵĹ��ת��Ч�ʶ���̫���ܵ�����������Ҫ��Ӧ�ü�ֵ���ش���������
��1��C��N��̬ԭ���У���һ�����ܽϴ����_____��
��2��CH3NH3+�ĵ���ʽΪ_____��C��Nԭ�ӵ��ӻ�������ͷֱ�Ϊ______��______��CH3NH3+�У�����______������ţ���
a������ b������ c����� d�����
��֪���Ĺ���������ǿ����ԭ�ӣ���CH3NH2��(CH3)2NH�н�������������ǿ����______��
��3��(CH3NH3)PbI3����������ṹ��ͼ��ʾ������B����Pb2+����______���� I��ÿ�������к���I ����ĿΪ______��ԭ�ӷ�����������ڱ�ʾ�����ڲ���ԭ�ӵ����λ�á����У�ԭ�ӷ�������AΪ��0��0��0����BΪ��1/2��1/2��1/2������C��ԭ�ӷ�������Ϊ______����֪(CH3NH3)PbI3�ľ�������Ϊa pm�������ܶ�Ϊ g��cm3����NAΪ�����ӵ�������ֵ����(CH3NH3)PbI3��Ħ������Ϊ________g��mol1���ô���ʽ��ʾ����
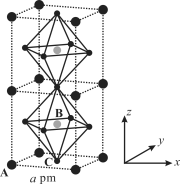
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷��Ѵ�����ұ��������ķ�������Ҫ��FeO��V2O3��Al2O3��SiO2�����������������Σ�����V2O5�Ĺ����������£��ش��������⣺
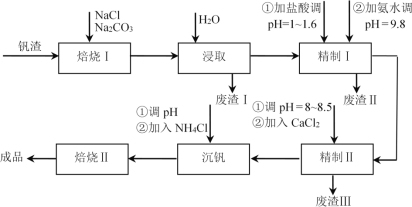
��֪����V2O5��Al2O3��SiO2����Na2CO3��NaCl��ɵĻ�������ڸ����·�Ӧ����ת��ΪNaVO3��NaAlO2��Na2SiO3�ȿ��������Ρ�
��AlO![]() +4H+=Al3++2H2O��
+4H+=Al3++2H2O��
��1�����բ�����������ƻ������������̣�������Ŀ���ǻ��V2O5��д������������FeO��V2O3������Ӧ�Ļ�ѧ����ʽ________�����������Ҫ�ɷ���________�����Ƣ��м������pH����Ҫ������________������NH3��H2O������Ӧ�����ӷ���ʽΪ________��
��2�����Ƣ��м���CaCl2��Һ��ȥ�����Σ�pH��СʱӰ�����Ч����ԭ����________��pH����ʱ�������������ԭ����________��
��3����������NH4VO3���������ϴ�ӣ�ϴ��ʱ��ȥ����������Ҫ��________��NH4VO3��500��ʱ�����Ѱ��Ƶò�ƷV2O5����Ӧ����ʽΪ2NH4VO3![]() V2O5+H2O��+2NH3�������Ѱ������У�����V2O5��ת����V2O4����Ӧ���������뻹ԭ�����ʵ���֮��Ϊ3:2���÷�Ӧ�Ļ�ѧ����ʽΪ________��
V2O5+H2O��+2NH3�������Ѱ������У�����V2O5��ת����V2O4����Ӧ���������뻹ԭ�����ʵ���֮��Ϊ3:2���÷�Ӧ�Ļ�ѧ����ʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵�����ʾ��������ȷ����
A. ������ȼ����Ϊ285.8 kJ��mol��1��������ȼ�յ��Ȼ�ѧ����ʽΪ2H2(g)��O2(g)=2H2O(l) ��H����285.8 kJ��mol��1
B. ������������������۷ֱ���ȫȼ�գ����߷ų���������
C. ij�ܱ�����ʢ��0.1 mol N2��0.3 mol H2����һ�������³�ַ�Ӧ,ת�Ƶ��ӵ���ĿС��0.6��6.02��1023
D. ��֪�к���Ϊ57.3 kJ��mol��1��������0.5 mol H2SO4��Ũ������Һ�뺬1 mol NaOH����Һ��ϣ��ų�������ҪС��57.3 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������������������ԭ�������͵���
A. ʵ�������ű���ʳ��ˮ�ķ����ռ�����
B. ��ˮ��������ƽ��Br2+H2O![]() HBr+HBrO����������������Һ��AgBr�ǵ���ɫ����������Һ��ɫ��dz
HBr+HBrO����������������Һ��AgBr�ǵ���ɫ����������Һ��ɫ��dz
C. SO2��������SO3�Ĺ�����ʹ�ù���������������߶��������ת����
D. ���¡���ѹ�����£���2NO2![]() N2O4ƽ����ϵ�г���He����ϵ��ɫ��dz
N2O4ƽ����ϵ�г���He����ϵ��ɫ��dz
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��pKa=-lgKa��25��ʱ H2A ��pKa1=1.85��pKa2=7.19�������£��� 0.1mol��L-1NaOH �ܷ�Һ�ζ� 20 mL 0.1 mol��L-1H2A ��Һ�ĵζ�������ͼ��ʾ������˵������ȷ����
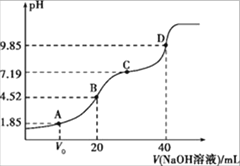
A.A �� V0��10 mL��
B.B ��������Һ�У�c(H2A)+c(H+)=c(HA-)+c(OH-)
C.C ��������Һ�У�c(A2-)=c(HA-)
D.D ��������Һ�У�A2-ˮ��ƽ�ⳣ��Kh1=10-6.81
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ����ˮ��ɹ�ɵô��Σ����γ�NaCl�⣬������MgCl2��CaCl2��Na2SO4�Լ���ɳ�����ʣ��������Ʊ����ε�ʵ�鷽�������������������£�
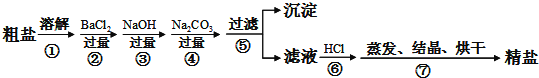
��1���ڢڲ�������Ŀ���dz�ȥ�����е�______���ѧʽ����
��2���ڢݲ��������������еõ������ijɷ��У���ɳ��BaSO4��Mg��OH��2��CaCO3��___���ѧʽ����
��3���ڵڢ۲������У�ѡ��ij����Լ�������KOH����NaOH��������________��
��4��д���ڢ���Ӧ�����ӷ���ʽ_______________,______________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com