
下列反应既属于氧化还原反应,又是吸热反应的是
A.锌粒与稀硫酸的反应 B.灼热的木炭与CO2的反应
C.乙醇在氧气中燃烧 D.Ba(OH)2·8H2O晶体与NH4Cl晶体反应
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源:2015-2016学年广东省高一下期中化学试卷(解析版) 题型:选择题
某烃含碳元素的质量分数为85.7 %,则该烃是
A.甲烷 B.乙烯 C.苯 D.不能确定
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:选择题
下列物质与类类别不对应的是
A | B | C | D |
小苏打
| 食用油
| 淀粉
| 84消毒液
|
盐 | 高分子化合物 | 糖类 | 混合物 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西河池高中高一下第二次月考化学试卷(解析版) 题型:选择题
近年来,广州市的大部分公交车及部分出租车己采用LPG (液化石油气)作为汽车的燃料,其主要目的是( )
A.防止石油短缺 B.降低成本 C.减少对大气的污染 D.加大发动机的动力
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:计算题
将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)=xC(g)+2D(g)经5分钟后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率是0.1mol/(L.min)。求:
(1)此时A的浓度c(A)= mol/L,反应开始前容器中A、B的物质的量为 mol.
(2)B的平均反应速率v(B)= mol/(L.min)。
(3)B的转化率为 。
(4)x= 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
有下列两种转化途径,某些反应条件和产物已省略。下列有关说法不正确的是
途径① S H2SO4
H2SO4
途径② S SO2
SO2 SO3
SO3 H2SO4
H2SO4
A.途径①反应中体现了浓硝酸的强氧化性和酸性
B.途径②的第二步反应在实际生产中可以通过增大O2浓度来降低成本
C.由途径①和②分别制取1 mol H2SO4,理论上各消耗1 mol S,各转移6 mol e-
D.途径②与途径①相比更能体现“绿色化学”的理念是因为途径②比途径①污染相对小且原子利用率高
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
氰气的化学式为(CN)2,它的性质和卤素相似,称为拟卤素,对其性质和有关化合物性质的叙述不正确的是
A.NaCN和AgCN都易溶于水
B.HCl和HCN都易形成白雾
C.MnO2可与HCN反应生成(CN)2
D.(CN)2和NaOH溶液反应生成NaCN、NaCNO和H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:填空题
Ⅰ、按要求书写下列化学方程式和名称:
(1)1,3-丁二烯与等物质的量的单质溴在60℃时发生1,4-加成
(2)甲苯制备TNT ,用系统命名给TNT命名
(3)乙醛发生银镜反应
Ⅱ、(1)某烃A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,与氢气加成反应可得到结构简式为(CH3)2CHCH(CH3)2的烷烃,则此烯烃可能的结构简式是: (任写一种)。
(2)核磁共振谱表明A分子中只有一种类型的氢。
①用系统命名法给A命名: 。
②A中的碳原子是否都处于同一平面? (填“是”或者“不是”)。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三第五次模拟理综化学试卷(解析版) 题型:填空题
氢气是清洁的能源,也是重要的化工原料,根据以下两种制氢方法。完成下列问题:
(1)方法一:H2S热分解法,反应式为:2H2S(g)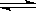 2H2(g)+S2(g)△H
2H2(g)+S2(g)△H
在恒容密闭容器中,测定H2S分解的转化率(H2S的起始浓度均为cmol/L),测定结果见右图,图中曲线a表示H2S的平衡转化率与温度关系,曲线表示不同温度下反应经过相同时间未达到化学平衡时H2S的转化率。
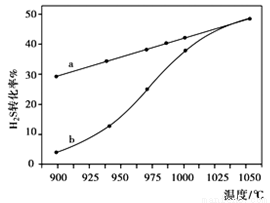
①△H______0,(“>”、“<”或“=”),
②若985℃时,反应经tmin达到平衡,此时H2S的转化率为40%,则tmin内反应速率v(H2)=______(用含c、t的代数式表示)。
③请说明随温度的升高,曲线b向曲线a接近的原因:______。
(2)方法二:以CaO为吸收体,将生物材质(以C计)与水蒸气反应制取H2.相关主要反应如下:
I:C(s)+H2O(g)═CO(g)+H2(g) △H=+131.0kJ/mol
Ⅱ:CO(g)+H2O(g)═CO2(g)+H2(g) △H=-43kJ/mol
Ⅲ:CaO(s)+CO2(g)═CaCO3(s) △H=-178.3kJ/mol
①计算反应C(s)+2H2O(g)+CaO(s)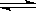 CaCO3(s)+2H2(g)的△H=______;
CaCO3(s)+2H2(g)的△H=______;
若K1、K2、K3分别为反应I、Ⅱ、Ⅲ的平衡常数,该平衡常数K=_____________(用K1、K2、K3表示)。
②对于可逆反应C(s)+2H2O(g)+CaO(s)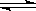 CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是______。(填字母编号)
CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是______。(填字母编号)
A.降低体系的温度
B.压缩容器的体积
C.适当增加水蒸气的通入量
D.增加CaO的量
③下图为反应I在一定温度下,平衡时各气体体积百分含量随压强变化的关系图。若反应达某一平衡状态时,测得c(H2O)=2c(H2)=2c(CO)=2mol/L,试根据H2O的体积百分含量变化曲线,补充完整CO的变化曲线示意图。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com