
| A. | 58.5gNaCl溶于1L水中,形成溶液浓度为1 mol•L-1 | |
| B. | 将Na2O和Na2O2各1mol溶于水配成1L溶液,所得溶液物质的量浓度不同 | |
| C. | 标况下22.4LNH3溶于水配成1L溶液,所得溶液浓度为1 mol•L-1 | |
| D. | 要配制100mL1 mol•L-1的硫酸铜溶液,需要胆矾1.6g |
分析 A.氯化钠溶于1L水中,所得溶液的体积不是1L;
B.1mol氧化钠和过氧化钠与水反应都生成2mol氢氧化钠,所得溶液浓度都是2mol/L;
C.标准状况下22.4L氨气的物质的量为1mol,所得溶液浓度为1mol/L;
D.根据n=cV计算出硫酸铜的物质的量,然后根据m=nM计算出胆矾的质量.
解答 解:A.58.5gNaCl溶于1L水中,所得溶液体积不是1L,则形成溶液浓度不是1 mol•L-1,故A错误;
B.将Na2O和Na2O2各1mol溶于水配成1L溶液,所得溶液中氢氧化钠的浓度都是2mol,所得溶液物质的量浓度都是2mol/L,故B错误;
C.标况下22.4LNH3的物质的量为:$\frac{22.4L}{22.4L/mol}$=1mol,1mol氨气溶于水配成1L溶液,所得溶液浓度为1 mol•L-1,故C正确;
D.100mL1 mol•L-1的硫酸铜溶液中含有硫酸铜的物质的量为:1mol/L×0.1L=0.1mol,0.1mol胆矾的质量为:250g/mol×0.1mol=25.0g,故D错误;
故选C.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确物质的量与摩尔质量、物质的量浓度之间的关系为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
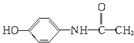 .下列有关该有机物叙述正确的是( )
.下列有关该有机物叙述正确的是( )| A. | 分子式为C8H10NO2 | |
| B. | 其属于α-氨基酸的同分异构体有3种 | |
| C. | 该有机物属于α-氨基酸 | |
| D. | 该有机物可与FeCl3溶液发生显色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
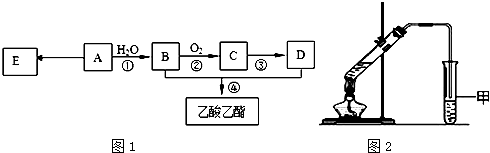
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器中CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1 | |
| B. | v正(CO2)=3v逆(H2) | |
| C. | 容器内混合气体平均相对分子质量保持不变 | |
| D. | 容器中CO2、H2、CH3OH、H2O的物质的量浓度都相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +3 | B. | +4 | C. | +5 | D. | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌 | |
| B. | 含I-的滤液中加入稀硫酸和双氧水后,碘元素发生还原反应 | |
| C. | 在碘水中加入几滴淀粉溶液,溶液出现蓝色沉淀 | |
| D. | 碘水加入CCl4得到I2的CCl4溶液,该操作为萃取 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,33.6 L氯气与27 g铝充分反应,转移电子数为3NA | |
| B. | 标准状况下,分子数为NA的CO、N2混合气体体积为22.4 L,其质量为28 g | |
| C. | 50 mL 8 mol•L-1的浓盐酸与足量的MnO2加热反应,生成Cl2的分子数为0.1NA | |
| D. | 标准状况下,80 g SO3中含3NA个氧原子,体积为22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 铜棒为负极 | B. | 锌棒发生氧化反应 | ||
| C. | 锌棒质量减轻 | D. | 电子从锌棒经外电路流向铜棒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com